يرجى استخدام متصفح الكمبيوتر الشخصي للوصول إلى التسجيل - تداول السعودية
أعلنت شركة Fractyl Health عن نتائج ما قبل السريرية الفعالة لـ RJVA-002، وهو مرشح لعلاج السمنة بجينات GIP/GLP-1 المزدوجة
Fractyl Health, Inc. GUTS | 0.49 0.49 | +1.88% 0.00% Pre |
حقق RJVA-002 فقدانًا للوزن بنسبة 30% تقريبًا في خمسة أسابيع في نموذج السمنة الانتقالية؛ ولم يصل فقدان الوزن إلى ذروته بعد
تظهر النتائج السريرية الأولية أن علاجًا واحدًا في وقت واحد باستخدام RJVA-002 لديه القدرة على تحقيق فقدان كبير للوزن يمكن أن يطابق أو يتجاوز أفضل علاج دوائي مزمن في فئته
برلنغتون، ماساتشوستس، 7 أكتوبر/تشرين الأول 2025 (جلوب نيوز واير) - أعلنت اليوم شركة فراكتيل هيلث (المدرجة في بورصة ناسداك تحت الرمز: GUTS)، وهي شركة متخصصة في العلاجات الأيضية تُركز على مناهج مبتكرة لعلاج الأسباب الجذرية للسمنة وداء السكري من النوع الثاني، عن بيانات ما قبل سريرية جديدة فعّالة لدواء RJVA-002، وهو الدواء الثاني المُرشَّح من منصة Rejuva ® Smart GLP-1 ™ الخاصة بالشركة، وذلك خلال مؤتمر الخلايا والجينات 2025 في ميسا. تُوسِّع هذه البيانات الجديدة إمكانات منصة Rejuva من العلاج طويل الأمد لداء السكري من النوع الثاني إلى علاج السمنة.
يُشفِّر RJVA-002 كلاً من هرموني GIP وGLP-1، ويدفعه مُحفِّز إنسولين بشري مُهندَس وراثيًا لتمكين التعبير المُستجيب للمغذيات والمُخصَّص لخلايا بيتا. في نموذج فأر مُصاب بالسمنة المُستحثة بالنظام الغذائي (DIO) مع مُستقبِل GIP مُؤنسن، أدت جرعة واحدة من RJVA-002 إلى فقدان حوالي 30% من الوزن على مدار 5 أسابيع، مع عدم استقرار مسار فقدان الوزن بعد. لم تُلاحظ أي آثار جانبية في الحيوانات المُعالَجة. تُشير هذه النتائج إلى نشاط قوي ودائم في نموذج السمنة المُستحث بالنظام الغذائي ذي الصلة الانتقالية، مما يدعم إمكانات المنصة كبديل من الجيل التالي للعلاج الدوائي المُزمن للسمنة.
قال الدكتور هاريث راجاجوبالان، المؤسس المشارك والرئيس التنفيذي لشركة فراكتيل هيلث: "تدعم بيانات RJVA-002 نهجنا في منصة العلاج الجيني Smart GLP-1، وتشير إلى أن التعبير المزدوج للهرمون المعوي لديه القدرة على إحداث تأثيرات أيضية قوية". وأضاف: "إلى جانب بيانات REMAIN-1 التي تم الإبلاغ عنها مؤخرًا، ومع اقتراب RJVA-001 من مرحلة التجارب السريرية في عام 2026، تؤكد هذه النتائج قوة وتنوع محفظتنا العلاجية. نحن نطور استراتيجية متعددة الوسائط بهدف تحويل نموذج علاج السمنة وداء السكري من النوع الثاني من إدارة الأمراض المزمنة إلى علاج دائم للمرض".
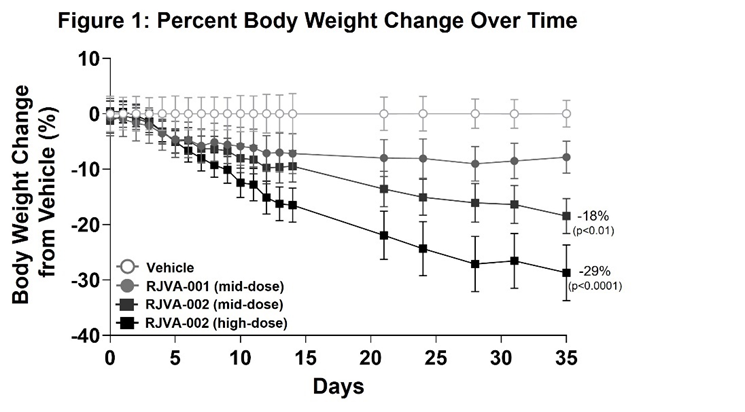
في هذه الدراسة ما قبل السريرية الجارية، أُطعمت فئران ذكور مُعدّلة وراثيًا للتعبير عن مستقبل GIP مُؤنسن (Biocytogen) نظامًا غذائيًا عالي الدهون بنسبة 60% لتحفيز السمنة، ثم وُزّعت عشوائيًا على أربع مجموعات علاجية: مجموعة التحكم، ومجموعة RJVA-001 بجرعة متوسطة، ومجموعة RJVA-002 بجرعة متوسطة، ومجموعة RJVA-002 بجرعة عالية (عدد الفئران = 7 لكل مجموعة). استمرّت جميع الفئران على نظام HFD طوال مدة الدراسة. أدى العلاج بـ RJVA-002 إلى انخفاض كبير في وزن الجسم يعتمد على الجرعة مقارنةً بمجموعة التحكم (الشكل 1). بحلول اليوم 35، فقدت الفئران في مجموعتي الجرعات المتوسطة والعالية متوسط 18% (p<0.01) و29% (p<0.0001) من وزن الجسم بعد جرعة واحدة من RJVA-002، على التوالي (الشكل 1).
سيتم عرض نتائج هذه الدراسة المستمرة في نقاط زمنية أطول مع القياسات الأيضية المرتبطة بها في مؤتمر علمي قادم.
ريجوفا هي منصة العلاج الجيني من شركة فراكتيل، المصممة لتمكين شفاء طويل الأمد من داء السكري من النوع الثاني والسمنة، وذلك بإعادة برمجة خلايا جزر البنكرياس بشكل مستدام لإنتاج هرمونات أيضية ذاتيًا. من المتوقع أن يدخل RJVA-001، أول مرشح لريجوفا، أولى التجارب السريرية على البشر في عام 2026 للمرضى الذين يعانون من داء السكري من النوع الثاني غير المسيطر عليه بشكل كافٍ. يوسع RJVA-002 نطاق المنصة ليشمل السمنة، مستهدفًا بيولوجيا الإنكريتين المزدوج بهدف تحقيق فقدان وزن مستدام وجيد التحمل من خلال تدخل واحد.
العرض التقديمي متاح عبر قسم علاقات المستثمرين بموقع Fractyl الإلكتروني.
نبذة عن Fractyl Health
فراكتيل هيلث هي شركة متخصصة في العلاجات الأيضية، تُركز على ابتكار مناهج جديدة لعلاج الأمراض الأيضية، بما في ذلك السمنة وداء السكري من النوع الثاني. على الرغم من التقدم المحرز في العلاج على مدى الخمسين عامًا الماضية، لا تزال السمنة وداء السكري من النوع الثاني يُشكلان عوامل نمو سريعة للمرض والوفيات في القرن الحادي والعشرين. تهدف فراكتيل إلى تحويل علاج الأمراض الأيضية من إدارة الأعراض المزمنة إلى علاجات مُعدّلة للمرض، تستهدف الأسباب الجذرية للمرض على مستوى الأعضاء. تمتلك الشركة محفظة قوية ومتنامية من براءات الاختراع، حيث حصلت على 33 براءة اختراع أمريكية مُنحت، وحوالي 40 طلبًا أمريكيًا قيد الانتظار، بالإضافة إلى العديد من براءات الاختراع الصادرة عن جهات خارجية والطلبات قيد الانتظار. يقع مقر فراكتيل في برلنغتون، ماساتشوستس. لمزيد من المعلومات، يُرجى زيارة الموقع الإلكتروني www.fractyl.com .
نبذة عن ريجوفا ®
تُركز منصة ريجوفا من شركة فراكتيل هيلث على تطوير الجيل التالي من العلاجات الجينية المُوَصَّلة محليًا، القائمة على فيروس الغدة الدرقية المرتبط (AAV)، لعلاج السمنة وداء السكري من النوع الثاني. لا تزال منصة ريجوفا في مرحلة التطوير ما قبل السريري، ولم تُقيَّم بعد من قِبَل الهيئات التنظيمية للاستخدام التجريبي أو التجاري. تستفيد ريجوفا من أنظمة توصيل متطورة وأساليب فحص خاصة لتحديد وتطوير علاجات جينية مُرشَّحة نشطة أيضيًا تستهدف البنكرياس. يهدف البرنامج إلى إحداث نقلة نوعية في إدارة الأمراض الأيضية من خلال تقديم علاجات جديدة مُعَدِّلة للمرض، تُعالج الأسباب الجذرية الكامنة وراءه. قدمت الشركة أول وحدة طلب تجربة سريرية (CTA) لـ RJVA-001 في داء السكري من النوع 2 إلى الجهات التنظيمية، وإذا تمت الموافقة على CTA، تتوقع الشركة إعطاء الجرعة الأولى من RJVA-001 للمرضى والإبلاغ عن البيانات الأولية في عام 2026. RJVA-002، المرشح الثاني للشركة من منصة Rejuva، هو علاج جيني مزدوج GIP / GLP-1 للسمنة أظهر فقدانًا للوزن بنسبة 30٪ تقريبًا في الدراسات السريرية قبل السريرية بعد جرعة واحدة، مما يؤكد قدرته على تقديم فوائد أيضية دائمة ومتحملة جيدًا من تدخل لمرة واحدة.
نبذة عن ريفيتا ®
يعتمد منتج "ريفيتا"، المرشح الرئيسي لشركة "فراكتيل هيلث"، على رؤى الشركة حول الدور المحتمل للأمعاء في السمنة. صُمم "ريفيتا" لإعادة تشكيل بطانة الاثني عشر عبر الاستئصال الحراري المائي (أي تجديد سطح الغشاء المخاطي للاثني عشر) لعكس الضرر الذي يلحق بآليات استشعار المغذيات والإشارات المعوية الناتجة عن اتباع نظام غذائي مزمن غني بالدهون والسكريات، والذي يُعدّ سببًا رئيسيًا لأمراض التمثيل الغذائي. في الولايات المتحدة، يُستخدم "ريفيتا" لأغراض بحثية فقط بموجب القانون الأمريكي. حصل "ريفيتا" على تصنيف "جهاز مبتكر" من إدارة الغذاء والدواء الأمريكية (FDA) للحفاظ على الوزن للأشخاص الذين يعانون من السمنة والذين يتوقفون عن تناول أدوية GLP-1. بدأت دراسة محورية لـ"ريفيتا" على مرضى السمنة بعد التوقف عن تناول أدوية GLP-1، تُسمى "ريماين-1"، في الربع الثالث من عام 2024، وقد اكتمل تسجيل المشاركين فيها.
تصريحات تطلعية
يحتوي هذا البيان الصحفي على بيانات تطلعية ضمن معنى قانون إصلاح التقاضي للأوراق المالية الخاصة لعام 1995. يجب اعتبار جميع البيانات الواردة في هذا البيان الصحفي والتي لا تتعلق بمسائل الحقائق التاريخية بيانات تطلعية، بما في ذلك، على سبيل المثال لا الحصر، البيانات المتعلقة بالوعد والتأثير المحتمل لبيانات التجارب السريرية أو ما قبل السريرية لدينا، والتصميم، والبدء، والتوقيت، ونقاط النهاية الأولية والثانوية، ونتائج التسجيل السريري وأي دراسات أو قراءات سريرية، والمحتوى أو المعلومات المستخدمة أو توقيت أو نتائج أي دراسات تمكينية لأدوية جديدة تجريبية (IND)، وتطبيقات IND أو تطبيقات التجارب السريرية، والاتصالات مع الجهات التنظيمية، والإطلاق المحتمل أو التسويق التجاري لأي من مرشحي منتجاتنا أو منتجاتنا، وسكان العلاج المحتملين أو الفوائد لأي من مرشحي منتجاتنا أو منتجاتنا، وأهدافنا الاستراتيجية وتطوير المنتجات، بما في ذلك فيما يتعلق بتمكين السيطرة طويلة المدى على السمنة ومرض السكري من النوع 2 دون عبء العلاجات المزمنة، وإعادة تعريف مستقبل علاج الأمراض الأيضية، ووضع شركتنا في طليعة الفرصة العالمية لرعاية التمثيل الغذائي، و توقيت أي مما سبق. هذه البيانات ليست وعودًا ولا ضمانات، ولكنها تنطوي على مخاطر معروفة وغير معروفة، وعدم يقين وعوامل مهمة أخرى قد تتسبب في اختلاف النتائج أو الأداء أو الإنجازات الفعلية للشركة ماديًا عن أي نتائج أو أداء أو إنجازات مستقبلية صريحة أو ضمنية من خلال البيانات التطلعية، بما في ذلك على سبيل المثال لا الحصر ما يلي: تاريخ التشغيل المحدود للشركة؛ تكبد خسائر صافية كبيرة وحقيقة أن الشركة تتوقع الاستمرار في تكبد خسائر صافية كبيرة في المستقبل المنظور؛ حاجة الشركة إلى تمويل إضافي كبير؛ قدرة الشركة على الاستمرار ككيان مستمر؛ الشروط التقييدية والمالية في اتفاقية ائتمان الشركة؛ عملية الموافقة التنظيمية الطويلة وغير المتوقعة لمرشحي منتجات الشركة؛ عدم اليقين بشأن دراساتها السريرية؛ حقيقة أن مرشحي منتجات الشركة قد يتسببون في أحداث سلبية خطيرة أو آثار جانبية غير مرغوب فيها أو لديهم خصائص أخرى قد تتسبب في تعليق أو إيقاف الدراسات السريرية أو تأخير أو منع التطوير التنظيمي أو منع الموافقة التنظيمية عليها أو الحد من الملف التجاري أو التسبب في عواقب سلبية كبيرة؛ قد يلزم وقت إضافي لتطوير والحصول على موافقة تنظيمية أو شهادة لمرشحي العلاج الجيني Rejuva للشركة؛ اعتماد الشركة على أطراف ثالثة لإجراء جوانب معينة من الدراسات السريرية وما قبل السريرية للشركة؛ اعتماد الشركة على أطراف ثالثة لتصنيع المواد اللازمة لمنصة العلاج الجيني Rejuva للدراسات ما قبل السريرية ودراساتها السريرية الجارية؛ عملية الموافقة التنظيمية من قبل إدارة الغذاء والدواء، والسلطات التنظيمية الأجنبية المماثلة، وهي عملية طويلة وتستغرق وقتًا طويلاً وغير متوقعة بطبيعتها، وحتى إذا أكملنا الدراسات السريرية اللازمة، لا يمكننا التنبؤ بموعد أو ما إذا كنا سنحصل على موافقة تنظيمية أو شهادة لأي من مرشحي منتجاتنا، وقد تكون أي موافقة أو شهادة تنظيمية من هذا القبيل لمؤشر أضيق مما نسعى إليه؛ والإطلاق أو التسويق المحتمل لأيٍّ من منتجات الشركة المرشحة أو منتجاتها، وأهدافنا الاستراتيجية وأهداف تطوير المنتجات، والعوامل الأخرى التي نوقشت تحت عنوان "عوامل الخطر" في تقريرنا الفصلي على النموذج 10-Q المقدم إلى هيئة الأوراق المالية والبورصات الأمريكية (SEC) بتاريخ 12 أغسطس 2025، وفي ملفاتنا الأخرى المقدمة إلى الهيئة. تستند هذه البيانات التطلعية إلى تقديرات وتوقعات الإدارة الحالية. مع أن الشركة قد تختار تحديث هذه البيانات التطلعية في وقت ما مستقبلًا، إلا أنها تُخلي مسؤوليتها عن أي التزام بذلك، حتى لو أدت أحداث لاحقة إلى تغيير وجهات نظرها.
جهات الاتصال
جهة الاتصال الإعلامية
جيسيكا كوترون، الاتصالات المؤسسية
jcotrone@fractyl.com، 978.760.5622
جهة اتصال المستثمر
بريان لوك، رئيس علاقات المستثمرين والتطوير المؤسسي
IR@fractyl.com، 951.206.1200
الصورة المرفقة بهذا الإعلان متاحة على الرابط التالي: https://www.globenewswire.com/NewsRoom/AttachmentNg/265dea50-4fff-4e1e-98d2-3a9c8b346220



