يرجى استخدام متصفح الكمبيوتر الشخصي للوصول إلى التسجيل - تداول السعودية
حققت شركة Immatics إثباتًا سريريًا لمفهوم خط أنابيب TCR ثنائي التخصص من الجيل التالي (TCER®) مع بيانات حول IMA402 (PRAME) وIMA401 (MAGEA4/8) وأعلنت عن خطوات التطوير التالية
Immatics N.V. IMTX | 9.81 9.51 | +6.17% -3.06% Pre |
ستستضيف الشركة مؤتمرًا عبر الهاتف وبثًا عبر الويب اليوم، 12 نوفمبر، الساعة 8:30 صباحًا بتوقيت شرق الولايات المتحدة/2:30 مساءً بتوقيت وسط أوروبا
- أظهرت مستقبلات الخلايا التائية ثنائية التخصص IMA402 وIMA401 تحملاً إيجابياً في RP2D بالإضافة إلى استجابات عميقة ودائمة في المرضى الذين خضعوا لعلاج مكثف مسبقًا في الخط الأخير مع مجموعة من الأورام الصلبة
- أدى IMA402 PRAME ثنائي التخصص في نطاق RP2D إلى نسبة استجابة 30% (6/20) في جميع المؤشرات، بما في ذلك 29% (4/14) في الورم الميلانيني و2/3 من الاستجابات المؤكدة في سرطان المبيض
- أدى IMA401 MAGEA4/8 ثنائي التخصص عند ≥1 مجم إلى معدل استجابة قلبية بنسبة 25% (2/8) في سرطان الرأس والرقبة، و29% (2/7) في الورم الميلانيني، ونشاط سريري واعد في سرطان الرئة ذو الخلايا غير الصغيرة.
- تم الانتهاء من تصعيد الجرعة في المرحلة 1أ لكلا التجربتين؛ تدعم البيانات فرص تطوير IMA402 PRAME ثنائي التخصص في سرطان الجلد والسرطانات النسائية وبالاشتراك مع IMA401 MAGEA4/8 ثنائي التخصص في سرطان الرئة ذو الخلايا غير الصغيرة (sqNSCLC)
- بدأت المرحلة 1ب من توسيع الجرعة لـ IMA402
- يمكن الوصول إلى المؤتمر الهاتفي والبث عبر الويب هنا
هيوستن ، تكساس وتوبينجن، ألمانيا، 12 نوفمبر 2025 - أعلنت اليوم شركة Immatics NV (المدرجة في بورصة ناسداك تحت الرمز: IMTX، أو "Immatics" أو "الشركة")، وهي شركة أدوية حيوية في المرحلة السريرية والرائدة عالميًا في الاستهداف الدقيق لـ PRAME، عن تحديث بيانات تصعيد الجرعة للمرحلة 1a من كلا المرشحين للمنتج في خط أنابيب TCR Bispecifics (TCER ® )، IMA402 PRAME Bispecific وIMA401 MAGEA4/8 Bispecific، بالإضافة إلى الخطوات التالية للتطوير السريري.
قال كارستن راينهاردت، الحاصل على دكتوراه في الطب، ورئيس قسم التطوير في شركة إماتكس: "تتميز مركباتنا ثنائية التخصص من مستقبلات الخلايا التائية الجاهزة للاستخدام بتركيبة خاصة من الجيل التالي مع إطالة عمر النصف، وهي مصممة للجمع بين قابلية تحمل مُحسّنة ونشاط قوي مضاد للأورام مع دعم جرعات مناسبة للمريض". وأضاف: "لقد حققنا الآن إثباتًا سريريًا لكلا المنتجين المرشحين، ورأينا إمكاناتهما في إحداث تأثير ملموس على المرضى ذوي خيارات العلاج المحدودة من خلال استجابات عميقة ودائمة. نتطلع إلى مواصلة تطوير مركباتنا ثنائية التخصص لتطوير علاجات مبتكرة وسهلة المنال، يمكنها الوصول إلى المزيد من المرضى وإحداث فرق دائم في رعاية مرضى السرطان".
قال الدكتور هاربريت سينغ، الرئيس التنفيذي والمؤسس المشارك لشركة إيماتكس: "يُمثل اليوم بداية مرحلة جديدة لشركة إيماتكس، حيث نوسع نطاقنا ليتجاوز العلاج الخلوي، ونرسخ مكانة رائدة في مجال مستقبلات الخلايا التائية ثنائية التخصص، مع التزام واضح بتطوير التطوير السريري لخط إنتاجنا من هذه الأدوية". وأضاف: "بناءً على هذه البيانات، يسعدنا تقييم منتجنا IMA402 PRAME ثنائي التخصص الآن على مجموعات متعددة من مرضى السرطان المستهدفين الذين لديهم احتياجات علاجية كبيرة لم تُلبَّ بعد، وباستخدام توليفات تآزرية محتملة. ونحن متحمسون بشكل خاص لإمكانية تحقيق فوائد كبيرة من خلال دمج IMA402 مع IMA401، وهو منتجنا MAGEA4/8 ثنائي التخصص، لدى مرضى سرطان الرئة الحرشفي ذي الخلايا غير الصغيرة، وهو مؤشر واسع الانتشار، ونادر العلاج، ويصعب علاجه".
سيقدم الدكتور كارستن راينهاردت، الحاصل على درجة الدكتوراه، والدكتور هاربريت سينغ، الحاصل على درجة الدكتوراه، مجموعة بيانات TCR Bispecifics الكاملة وخطوات التطوير التالية خلال مؤتمر هاتفي وبث مباشر عبر الإنترنت اليوم، 12 نوفمبر، الساعة 8:30 صباحًا بتوقيت شرق الولايات المتحدة/2:30 مساءً بتوقيت وسط أوروبا. يمكن الاطلاع على العرض التقديمي على صفحة " الفعاليات والعروض التقديمية " في قسم "المستثمرون والإعلام" على موقع الشركة الإلكتروني.
ملخص بيانات تصعيد الجرعة للمرحلة 1أ من دواء IMA402 PRAME ثنائي التخصص
فئة المرضى: أورام صلبة متقدمة لا تتوفر لها خيارات علاجية
اعتبارًا من تاريخ انتهاء البيانات في 26 سبتمبر 2025، عولج 80 مريضًا خضعوا لعلاج مكثف مسبقًا (بمتوسط ثلاث علاجات جهازية سابقة) مصابين بأورام صلبة متكررة و/أو مقاومة للعلاج 1 بجرعات متصاعدة من IMA402 أحادي العلاج تتراوح من 0.02 ملغ إلى 30 ملغ. تشمل فئة السلامة جميع المرضى الـ 80 الذين عولجوا بـ IMA402. تلقى 29 مريضًا جرعات في الجرعة الموصى بها من المرحلة الثانية (نطاق RP2D) (من 10 إلى 30 ملغ)، ومن بينهم 20 مريضًا قابلين لتقييم الفعالية 2 ، بما في ذلك 14 مريضًا مصابًا بالورم الميلانيني (12 جلديًا، وواحد عنبي، وواحد أولي غير معروف)، و3 مرضى مصابين بسرطان المبيض، و3 مرضى مصابين بسرطانات صلبة أخرى 3 .
السلامة: أظهر العلاج باستخدام IMA402 تحملاً إيجابياً
أظهر IMA402 تحمّلاً إيجابياً عبر نطاق واسع من الجرعات لدى 80 مريضاً عولجوا. كانت الآثار الجانبية الأكثر شيوعاً المرتبطة بالعلاج هي قلة اللمفاويات العابرة المتوقعة، بما يتوافق مع آلية العمل، ومتلازمة إطلاق السيتوكين منخفضة الدرجة (CRS): الدرجة 1: 33%، الدرجة 2: 5%، الدرجة 3: 0%، الدرجة 4: 1%. لم تحدث أي آثار جانبية من الدرجة 5 مرتبطة بـ ICANS أو IMA402. كان التحمّل لجميع الجرعات متسقاً مع التحمّل في نطاق RP2D.
تم الانتهاء من تصعيد جرعة المرحلة 1أ في العلاج الأحادي. لم يتم الوصول إلى الحد الأقصى للجرعة المسموح بها (MTD). تم تحديد النطاق المؤقت لـ RP2D عند 10 إلى 30 ملغ. ويجري حاليًا توسيع جرعة المرحلة 1ب بجرعتين منفصلتين ضمن نطاق RP2D، وبدأ تقييم استخدام IMA402 مع مثبط نقطة تفتيش مناعية.
النشاط المضاد للورم والمتانة: استجابات عميقة ودائمة لوحظت في نطاق RP2D
أظهر IMA402 علاقة واضحة بين الجرعة والاستجابة عبر ثلاث مجموعات جرعات مختلفة.
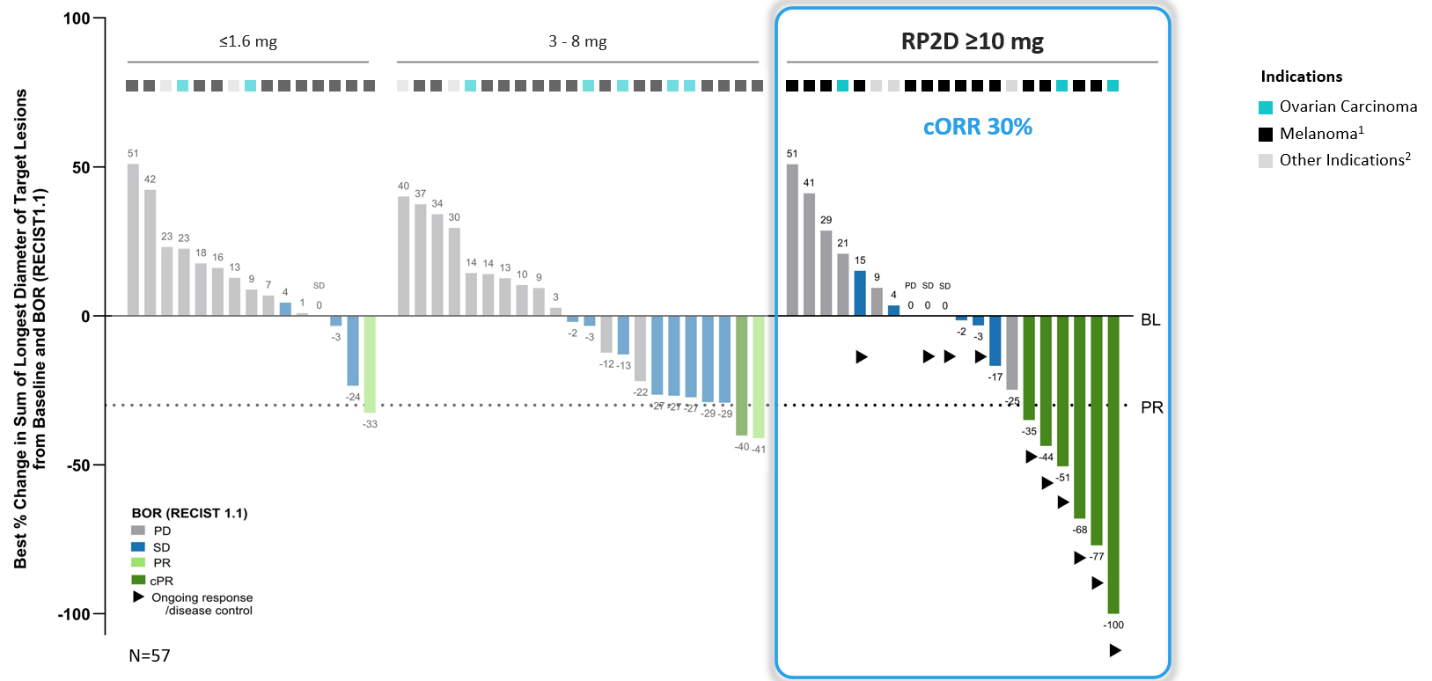
1- الورم الميلانيني يشمل الورم الميلانيني الجلدي، والورم الميلانيني الأولي غير المعروف، والورم الميلانيني العنبي؛ 2- تشمل المؤشرات الأخرى سرطان بطانة الرحم، والساركوما الزليلية، ومريض واحد مصاب بسرطان الرئة غير صغير الخلايا المتساوي بجرعة 1.6 ملغ؛ BL: خط الأساس؛ BOR: أفضل استجابة إجمالية؛ cORR : معدل استجابة موضوعي مؤكد؛ cPR : استجابة جزئية مؤكدة؛ PD: مرض متقدم؛ PR: استجابة جزئية ؛ SD: مرض مستقر؛ RECIST: معايير تقييم الاستجابة في الأورام الصلبة؛ RP2D: الجرعة الموصى بها من المرحلة الثانية
لوحظت استجابات عميقة ودائمة لدى العديد من المرضى الذين عولجوا بجرعة IMA402 عند نطاق RP2D. وكانت جميع الاستجابات الموضوعية الست المؤكدة مستمرة حتى تاريخ انتهاء البيانات، بما في ذلك استجابتان أيضيتان كاملتان في الورم الميلانيني الجلدي والعنقي، استمرتا عند عمر 8 و18 شهرًا على التوالي، بالإضافة إلى استجابة جزئية مؤكدة واحدة في سرطان المبيض مع انخفاض بنسبة 100% في الآفات المستهدفة. كان جميع المستجيبين المصابين بسرطان المبيض مقاومين للبلاتين، وكان جميع المستجيبين المصابين بالورم الميلانيني مقاومين لمثبطات نقاط التفتيش المناعية.
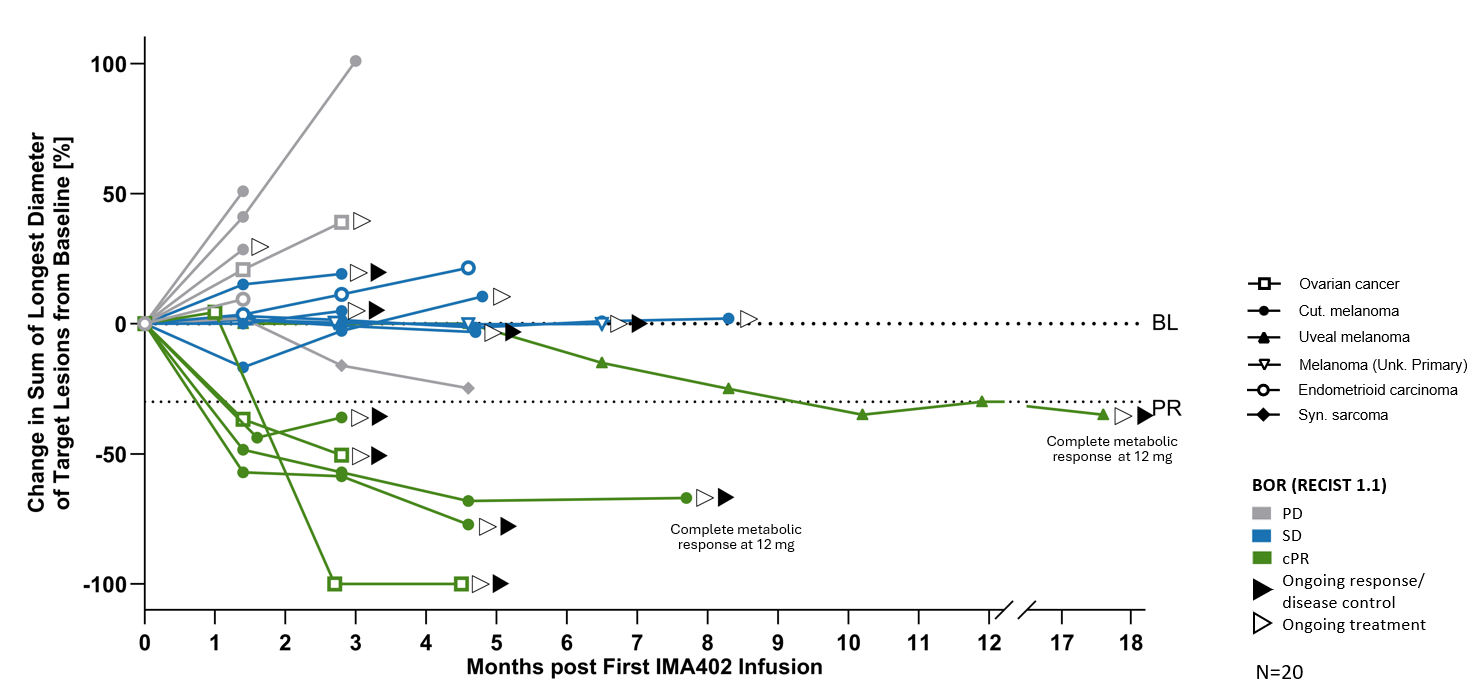
BL: خط الأساس؛ cPR: استجابة جزئية مؤكدة؛ PD: مرض متقدم؛ PR: استجابة جزئية؛ SD: مرض مستقر
استجابات عميقة ودائمة في نطاق RP2D (RECIST 1.1)
| الجميع دواعي الاستعمال | سرطان الجلد | المبيض سرطان | |
| كور | 30% (6/20) | 29% (4/14) | 2/3 |
| مدور، شهر mFU | لم يتم الوصول 4.2 | لم يتم الوصول 7.3 | لم يتم الوصول 2.2 |
| انكماش الورم | 55% (11/20) | 57% (8/14) | 2/3 |
| DCR (في الأسبوع 6) | 65% (13/20) | 71% (10/14) | 2/3 |
mDOR: متوسط مدة الاستجابة؛ mFU: متوسط المتابعة؛ DCR: معدل السيطرة على المرض
بالنسبة للمرضى الذين عولجوا في نطاق RP2D في وقت مبكر عبر جميع المؤشرات، لوحظت معدلات واعدة للبقاء على قيد الحياة دون تقدم (PFS) والبقاء على قيد الحياة بشكل عام (OS):
- كان متوسط البقاء خاليًا من التقدم 4.8 شهرًا عند متوسط عمر 6.8 شهرًا؛ وكان معدل البقاء خاليًا من التقدم لمدة 6 أشهر 45%
- لم يتم الوصول إلى متوسط iPFS 4 عند mFU لمدة 6.3 شهرًا؛ وكان معدل iPFS لمدة 6 أشهر 58%
- لم يتم الوصول إلى متوسط البقاء على قيد الحياة عند mFU لمدة 5.4 شهرًا؛ وكان معدل البقاء على قيد الحياة لمدة عام واحد 94%
فرص التطوير السريري لـ IMA402 PRAME ثنائي التخصص
بناءً على بيانات تصعيد الجرعة الواعدة للمرحلة 1أ، تعمل شركة إيماتكس على تطوير جرعة IMA402 PRAME ثنائية التخصص إلى المرحلة 1ب بجرعتين مختلفتين لتحديد الجرعة النهائية RP2D، سواءً كعلاج وحيد أو بالاشتراك مع مثبط نقطة تفتيش مناعية مع التركيز على سرطان الجلد وسرطانات النساء في عام 2026. بناءً على نتائج مجموعات المرحلة 1ب هذه، ستسعى الشركة إلى تحويل مجموعات المرحلة 1ب الحالية إلى تجارب المرحلة 2، والتي ستتمتع بعد ذلك بإمكانية أن تصبح موجهة للتسجيل. كجزء من استراتيجيتها لتعظيم فرصة IMA402، تدرس الشركة أيضًا خيار بدء مجموعات إضافية من المرحلة 1ب في عام 2026 لتحديد إمكانية العلاج الأحادي والجمع بين IMA402 ومثبطات نقطة التفتيش المناعية، ومعيار الرعاية في خطوط العلاج المتأخرة والمبكرة. كفرصة إضافية، تستكشف الشركة الجمع المحتمل بين IMA402 مع IMA401 MAGEA4/8 في سرطان الرئة ذو الخلايا غير الصغيرة الحرشفية (sqNSCLC) ومؤشرات الأورام الصلبة الأخرى المحتملة.
ملخص بيانات المرحلة 1أ ثنائية التخصص IMA401 MAGEA4/8
فئة المرضى: المرضى الذين تلقوا علاجًا مكثفًا مسبقًا مع مجموعة واسعة من أنواع الأورام دون خيارات علاجية متاحة
اعتبارًا من تاريخ انتهاء البيانات في 26 سبتمبر 2025، تم علاج 55 مريضًا خضعوا لعلاج مكثف مسبقًا (متوسط أربع علاجات جهازية سابقة) مصابين بأورام صلبة متكررة و/أو مقاومة 5 بمستويات جرعات متصاعدة من IMA401 تتراوح من 0.0066 ملغ إلى 2.5 ملغ مع أو بدون مثبط نقطة تفتيش مناعية (ICI، بيمبروليزوماب). تشمل مجموعة السلامة جميع المرضى البالغ عددهم 55 مريضًا الذين عولجوا بـ IMA401 كعلاج أحادي (ن = 46) أو بالاشتراك مع بيمبروليزوماب (ن = 9). عولج 44 مريضًا بجرعات تتراوح من 1 إلى 2.5 ملغ، وكان 38 منهم قابلين لتقييم الفعالية 6. جميع المرضى الذين يمكن تقييم فعاليتهم والذين عولجوا بـ IMA401 بالاشتراك مع بيمبروليزوماب (ن = 4) قد أحرزوا تقدمًا في علاجات مثبطات نقطة التفتيش المناعية السابقة.
السلامة: أظهر العلاج باستخدام IMA401 تحملاً إيجابياً في RP2D
كانت أكثر الآثار الجانبية شيوعًا وأهميةً المرتبطة بالعلاج لدى جميع المرضى الـ 55 الذين عولجوا بـ IMA401 هي متلازمة إطلاق السيتوكين منخفضة الدرجة (CRS) (24% في المرحلة الأولى، 11% في المرحلة الثانية، بدون ≥ الدرجة الثالثة)، ومعظمها عند الجرعة الأولى، وقلة لمفاوية متوقعة ومؤقتة، بما يتوافق مع آلية العمل، بالإضافة إلى قلة العدلات، والتي كانت في الغالب عابرة، ولا تتكرر بعد الشفاء مع استمرار العلاج، ويمكن التحكم بها جيدًا عند نطاق RP2D الذي يتراوح بين 1 و2 ملغ. والجدير بالذكر أنه لم يُلاحظ أي ICANS. تتوافق قابلية تحمل IMA401 مع بيمبروليزوماب مع قابلية تحمل IMA401 كعلاج وحيد.
لم يتم الوصول إلى الحد الأقصى للجرعة المسموح بها (MTD)؛ ولوحظت ثلاث حالات حدّت من الجرعة عند 2.5 ملغ. اكتملت عملية تصعيد الجرعة في المرحلة 1أ، وتم تحديد النطاق المؤقت لـ RP2D عند 1-2 ملغ. عند RP2D، كان نمط التحمل إيجابيًا.
النشاط المضاد للأورام والمتانة: لوحظ نشاط سريري واعد واستجابات عميقة ودائمة لدى المرضى المصابين بسرطان الرأس والرقبة وسرطان الجلد وسرطان الرئة الذين عولجوا بجرعة ≥ 1 ملغ
أظهر المرضى في ثلاثة مؤشرات تركيزية الذين عولجوا بجرعة ≥1 ملغ من IMA401 كعلاج وحيد أو بالاشتراك مع pembrolizumab نشاطًا سريريًا:
- سرطان الرأس والرقبة: معدل الاستجابة للمرض 25% (2/8)، معدل السيطرة على المرض 63% (5/8)
- الورم الميلانيني: معدل الاستجابة للورم 29% (2/7)، معدل السيطرة على المرض 57% (4/7)
- سرطان الرئة الحرشفي ذو الخلايا غير الصغيرة: استجابة جزئية واحدة في المسح الأول لمريض خضع لعلاج مكثف مسبقًا ومقاوم لـ ICI، ومريض واحد يعاني من مرض مستقر لأكثر من 4 أشهر وبقاء إجمالي لمدة 16 شهرًا تقريبًا، ومريض واحد يعاني من مرض متقدم مع انكماش آفات الكبد المستهدفة
كانت مدة جميع الاستجابات المؤكدة أطول من 6 أشهر بعد العلاج، مع استمرار أطول استجابة لأكثر من عامين في مريض مصاب بسرطان الجلد الميلانيني المتقدم.
فرصة التطوير السريري لـ IMA401 MAGEA4/8 ثنائي التخصص
تماشيًا مع تركيز شركة Immatics على تطوير امتياز PRAME الخاص بها، تستكشف الشركة استخدام IMA401 مع IMA402، بدءًا من سرطان الرئة الحرشفي ذي الخلايا غير الصغيرة (sqNSCLC). واستنادًا إلى نتائج الإثبات السريري لكلا العقارين ثنائيي التخصص، بما في ذلك النشاط الأولي الواعد لـ IMA401 في سرطان الرأس والرقبة وsqNSCLC، بالإضافة إلى بيانات الإثبات السريري قبل السريرية، تتمتع Immatics بمكانة جيدة لتقييم الإمكانات التآزرية لدمج عقارين ثنائيي التخصص مختلفين، IMA402 الذي يستهدف PRAME وIMA401 الذي يستهدف MAGEA4/8، مع أو بدون مثبط نقطة تفتيش. ونظرًا لأن أكثر من 90% من مرضى sqNSCLC إيجابيون لـ PRAME و/أو MAGEA4/8، فإن العلاج المُحتمل باستخدام IMA402 وIMA401 يُمكن أن يوفر تغطية علاجية واسعة لهذه الفئة من المرضى. حوالي 60% من مرضى سرطان الرئة ذو الخلايا غير الصغيرة المتسلسل (sqNSCLC) إيجابيون لكلا الهدفين، مما قد يعزز النشاط المضاد للأورام ويواجه آليات هروب الورم المحتملة. يشمل العدد الحالي للمرضى الذين يمكن علاجهم بسرطان الرئة ذو الخلايا غير الصغيرة المتسلسل (sqNSCLC) النقيلي في الولايات المتحدة وأوروبا الغربية (EU5) ما يُقدر بـ 40,000 مريض سنويًا.
نبذة عن Immatics TCR Biprofiles (TCER ® )
جزيئات TCER ® الممتدة لنصف العمر من الجيل التالي من Immatics هي مواد بيولوجية "جاهزة" تشبه الأجسام المضادة تعمل على تعزيز جهاز المناعة في الجسم عن طريق إعادة توجيه الخلايا التائية وتنشيطها نحو الخلايا السرطانية التي تعبر عن هدف ورمي محدد. يتيح تصميم جزيئات TCER ® تنشيط أي خلية تائية في الجسم لمهاجمة الورم، بغض النظر عن الخصوصية الجوهرية للخلايا التائية. تم تصميم المواد البيولوجية الخاصة بـ Immatics بمنطقتي ارتباط: نطاق TCR ونطاق تجنيد الخلايا التائية. تم تصميم صيغة TCER ® لزيادة الفعالية إلى أقصى حد مع تقليل السمية لدى المرضى. يحتوي على نطاق TCR عالي الألفة مصمم للارتباط بشكل خاص بببتيد هدف السرطان على سطح الخلية الذي يمثله جزيء HLA. يتم توجيه نطاق تجنيد الخلايا التائية منخفض الألفة المشتق من الأجسام المضادة ضد مركب TCR / CD3 ويجند الخلايا التائية للمريض إلى الورم لمهاجمة الخلايا السرطانية. باستخدام مُجنِّد منخفض الألفة يهدف إلى تحسين التوزيع الحيوي وإثراء الجزيء في موقع الورم بدلاً من محيطه، صُممت TCER ® لتقليل حدوث الآثار الجانبية المناعية، مثل متلازمة إطلاق السيتوكين. بالإضافة إلى ذلك، يتكون شكل TCER ® من جزء Fc يمنح إطالة عمر النصف، والاستقرار، وقابلية التصنيع. تُعدّ TCER ® من المستحضرات البيولوجية الجاهزة للاستخدام، وبالتالي فهي متاحة فورًا لعلاج المرضى. يمكن توزيعها عبر سلاسل توريد الأدوية القياسية، مما يتيح الوصول إلى شريحة كبيرة من المرضى دون الحاجة إلى مراكز طبية متخصصة.
نبذة عن PRAME
PRAME هو هدف مُعبَّر عنه في أكثر من 50 نوعًا من السرطان. تُعد شركة Immatics الشركة الرائدة عالميًا في مجال الاستهداف الدقيق لـ PRAME، وتمتلك أوسع امتياز لـ PRAME مع أكبر استخدامات وأساليب علاجية له. يضم امتياز Immatics PRAME حاليًا ثلاثة منتجات مرشحة، وأسلوبين علاجيين، وعلاجًا مركبًا يستهدف PRAME: علاج PRAME الخلوي anzu-cel (IMA203)، وعلاج PRAME الخلوي IMA203CD8 (GEN2)، وعلاج PRAME ثنائي التخصص IMA402، وanzu-cel مع مُحسِّن العلاج الخلوي PRAME من شركة Moderna.
حول IMA402 PRAME ثنائي التخصص
IMA402 هو جزيء من خط أنابيب TCR Bispecifics (TCER ® ) التابع لشركة Immatics والموجه ضد الببتيد المقدم من HLA-A*02:01 والمشتق من PRAME
يجري حاليًا تقييم IMA402 في تجربة من المرحلة الأولى على مرضى مصابين بأورام صلبة تُظهر جين PRAME. يُعد IMA402 جزءًا من استراتيجية Immatics للاستفادة من الإمكانات السريرية الكاملة لاستهداف PRAME، أحد أبرز الأهداف الواعدة للعلاجات القائمة على TCR.
حول IMA401 MAGEA4/8 ثنائي التخصص
IMA401 هو جزيء من خط إنتاج مستقبلات الخلايا التائية ثنائية الخصوصية من شركة Immatics، يستهدف ببتيدًا مُقدمًا بـ HLA-A*02:01، مشتقًا من بروتينين مختلفين مرتبطين بالسرطان، مستضد الورم الميلانيني 4 و/أو 8 ("MAGEA4/8"). تم تحديد ببتيد MAGEA4/8 والتحقق من صحته بواسطة منصة XPRESIDENT ® ، منصة اكتشاف الأهداف الخاصة بشركة Immatics والقائمة على مطياف الكتلة، ويتميز بكثافة هدف أعلى بخمسة أضعاف (عدد النسخ لكل خلية ورمية) من ببتيد MAGEA4 المُستهدف في تجارب سريرية أخرى.
يُقيَّم IMA401 حاليًا في تجربة سريرية من المرحلة الأولى على مرضى مصابين بأورام صلبة إيجابية لجين MAGEA4/8. يتميز ببتيد MAGEA4/8 بانتشار واسع في العديد من مؤشرات الأورام الصلبة، مثل سرطان الخلايا الحرشفية في الرأس والعنق (HNSCC)، وسرطان الرئة ذو الخلايا الحرشفية غير الصغيرة (sqNSCLC)، بالإضافة إلى الورم الميلانيني وأنواع أخرى من السرطانات الصلبة.
نبذة عن إيماتكس
تلتزم إيماتكس بإحداث تأثير ملموس في حياة مرضى السرطان. نحن الشركة الرائدة عالميًا في الاستهداف الدقيق لـ PRAME، وهو هدف يُعبّر عنه في أكثر من 50 نوعًا من السرطان. تُشكّل علومنا المتطورة ومسارنا السريري المتين أوسع امتياز لـ PRAME، مع أكبر عدد من دواعي استعماله وأساليبه العلاجية، بما في ذلك علاجات الخلايا التائية TCR ومضادات TCR ثنائية التخصص.
تعتزم شركة إيماتيكس استخدام موقعها الإلكتروني www.immatics.com كوسيلة للكشف عن معلومات جوهرية غير معلنة. للاطلاع على التحديثات الدورية، يمكنكم أيضًا متابعتنا على لينكدإن وإنستغرام .
تصريحات تطلعية
قد تُعتبر بعض البيانات الواردة في هذا البيان الصحفي بيانات تطلعية. تتعلق البيانات التطلعية عمومًا بالأحداث المستقبلية أو الأداء المالي أو التشغيلي المستقبلي للشركة. على سبيل المثال، البيانات المتعلقة بتوقيت قراءات بيانات المنتجات المرشحة، وملاحظات التجارب السريرية للشركة، وتوقيت التجارب السريرية ونتائجها وتصميمها، وطبيعة التجارب السريرية (بما في ذلك ما إذا كانت هذه التجارب ستُمكّن من التسجيل)، وتوقيت تقديم طلبات IND أو CTA أو BLA، والفرص السوقية المقدرة للمنتجات المرشحة، وتركيز الشركة على الشراكات لتعزيز استراتيجيتها، وغيرها من المقاييس، هي بيانات تطلعية. في بعض الحالات، يمكنك تحديد البيانات التطلعية من خلال مصطلحات مثل "قد"، "ينبغي"، "نتوقع"، "نخطط"، "نستهدف"، "ننوي"، "سوف"، "نقدر"، "نتوقع"، "نعتقد"، "نتنبأ"، "محتمل" أو "نستمر"، أو النفي لهذه المصطلحات أو صيغها المختلفة أو المصطلحات المماثلة. تخضع هذه البيانات التطلعية لمخاطر وعدم يقين وعوامل أخرى قد تؤدي إلى اختلاف النتائج الفعلية اختلافًا جوهريًا عن تلك الواردة صراحةً أو ضمنًا في هذه البيانات التطلعية. تستند هذه البيانات التطلعية إلى تقديرات وافتراضات، وإن اعتبرتها شركة Immatics وإدارتها معقولة، إلا أنها غير مؤكدة بطبيعتها. قد تظهر مخاطر وعدم يقين جديدة من وقت لآخر، وليس من الممكن التنبؤ بجميع المخاطر وعدم اليقين. تشمل العوامل التي قد تؤدي إلى اختلاف النتائج الفعلية اختلافًا جوهريًا عن التوقعات الحالية، على سبيل المثال لا الحصر، عوامل مختلفة خارجة عن سيطرة الإدارة، بما في ذلك الظروف الاقتصادية العامة والمخاطر وعدم اليقين والعوامل الأخرى الواردة في التقرير السنوي للشركة على النموذج 20-F والمستندات الأخرى المقدمة إلى هيئة الأوراق المالية والبورصات الأمريكية (SEC). لا ينبغي اعتبار أي شيء في هذا البيان الصحفي بمثابة إقرار من أي شخص بأن البيانات التطلعية الواردة فيه ستتحقق أو أن أيًا من النتائج المتوقعة لهذه البيانات التطلعية سيتحقق. يجب ألا تعتمد بشكل مفرط على البيانات التطلعية، التي تتحدث فقط عن تاريخ إصدارها. لا تلتزم الشركة بتحديث هذه البيانات التطلعية. جميع البيانات العلمية والسريرية الواردة في هذا البيان الصحفي - بحكم التعريف، قبل إتمام التجربة السريرية وتقرير الدراسة السريرية - أولية بطبيعتها، وتخضع لمزيد من فحوصات الجودة، بما في ذلك التحقق من بيانات المصدر المعتادة.
لمزيد من المعلومات، يرجى الاتصال بـ:
وسائط
الاتصالات الغذائية
الهاتف: +49 151 74416179
immatics@trophic.eu
إماتكس إن في
جوردان سيلفرشتاين
رئيس الاستراتيجية
الهاتف: +1 346 319-3325
علاقات المستثمرين@immatics.com
- نهاية -
1 الورم الميلانيني الجلدي، الورم الميلانيني العنبي، الساركوما الزليلية، سرطان بطانة الرحم، سرطان المبيض، سرطان الرئة ذو الخلايا غير الصغيرة الحرشفية.
2 مريض قابلين لتقييم الفعالية: جميع المرضى الذين عولجوا اعتبارًا من 26 يونيو 2025 (الذين أتيحت لهم الفرصة لمتابعة لمدة 3 أشهر على الأقل أو الذين توقفوا عن العلاج مبكرًا بسبب تطور المرض أو الوفاة)، ثبتت إصابتهم بـ PRAME أو لم يتم اختبارهم/غير قابلين للتقييم وتلقوا ≥4 دفعات كما هو محدد في البروتوكول (منها جرعات من 3 خطوات، حاليًا عند 0.03 مجم/0.3 مجم/6 مجم، وجرعة مستهدفة واحدة).
3 N = 2 سرطان بطانة الرحم، n = 1 ساركوما زليلية.
4. يُكيّف iRECIST، الذي طورته مجموعة عمل RECIST، تعريف RECIST 1.1 لتطور العلاجات المناعية من خلال إدخال تطور غير مؤكد (iUPD) ومؤكد (iCPD) لمراعاة أنماط الاستجابة غير النمطية. لا يُعتبر المرضى الذين يعانون من iUPD غير مؤكد في فحص لاحق، ولكنهم يتحولون إلى انحراف معياري أو استجابة، متطورين وفقًا لـ iRECIST. يُعرّف البقاء خاليًا من التقدم (PFS) (وفقًا لـ RECIST 1.1) والبقاء خاليًا من التقدم (iPFS) (وفقًا لـ iRECIST) كنقاط نهاية ثانوية مشتركة مُحددة استباقيًا في بروتوكول تجربة IMA402 لتوفير رؤية متوازنة للفعالية.
تجربة 5 سلة مع >15 مؤشرات مختلفة للورم.
6 مرضى قابلين لتقييم الفعالية: جميع المرضى الذين تم علاجهم اعتبارًا من 26 يونيو 2025 (الذين أتيحت لهم الفرصة لمتابعة لمدة 3 أشهر على الأقل أو الذين توقفوا عن العلاج مبكرًا بسبب تطور المرض أو الوفاة)، وتلقوا 4 دفعات أو أكثر كما هو محدد في البروتوكول (منها 3 جرعات متدرجة، حاليًا عند 0.3 مجم / 0.6 مجم / 1 مجم، وجرعة مستهدفة واحدة).
مرفق
- نسخة PDF



