أصدرت شركة ADMA Biologics بيانًا تنفي فيه الادعاءات التي لا أساس لها من الصحة والمضللة وغير الدقيقة التي قدمتها شركة Culper Research
ADMA Biologics, Inc. ADMA | 9.26 9.31 | -0.22% +0.51% Post |
إن وصف البائعين على المكشوف للوضع التنافسي لشركة ASCENIV يعكس سوء فهم صارخ لأعمال شركة ADMA ودورها كعلاج متأخر للمرضى الذين يعانون من ضعف المناعة، وبالتالي قد لا يستجيبون للقاحات.
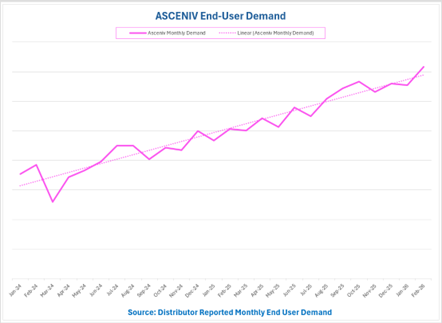
تُشير هذه النتائج إلى أن الطلب على منتج ASCENIV واستخدامه قد نما بشكل مطرد على مدار العامين الماضيين ووصل إلى مستوى قياسي.
توضح التفاصيل أن مستويات المخزون التي يحتفظ بها موزعو ADMA تتوافق مع معايير الصناعة وتعكس دورة الإنتاج الطويلة لـ ASCENIV
رامزي، نيوجيرسي وبوكا راتون، فلوريدا، 27 مارس 2026 (جلوب نيوزواير) - ردّت شركة ADMA Biologics, Inc. (ناسداك: ADMA) ("ADMA" أو "الشركة")، وهي شركة أمريكية متخصصة في مجال المستحضرات الصيدلانية الحيوية التجارية المتكاملة، والمتخصصة في تصنيع وتسويق وتطوير المستحضرات البيولوجية المتخصصة، اليوم على تقرير صادر في 24 مارس 2026 عن شركة كولبر ريسيرش، المتخصصة في البيع على المكشوف ("تقرير البيع على المكشوف"). وبعد مراجعة دقيقة لتقرير البيع على المكشوف، ترغب ADMA في دحض الادعاءات الرئيسية لتبديد أي لبس في السوق بشأن ممارسات الشركة وعملياتها التجارية.
تعتقد شركة ADMA أنه من خلال تقديم تفاصيل إضافية، على أساس غير متكرر، تتعلق بمجموعة منتجات الغلوبولين المناعي للشركة - بما في ذلك أيام المخزون المتوفرة لدى شركاء التوزيع والعملاء المباشرين، وبيانات طلب المستخدم النهائي - فإنها تدحض الادعاءات الكاذبة والمضللة الرئيسية الواردة في التقرير الموجز.
خاصة:
- الطلب على منتج ASCENIV حقيقي ومتزايد.
- كما يتضح من البيانات المقدمة مباشرة من شركاء التوزيع التابعين لشركة ADMA وعملائها المباشرين، فقد ازداد طلب المستخدم النهائي على ASCENIV على مدى العامين الماضيين.
- تُظهر مزاعم حشو القنوات سوء فهم للديناميكيات التجارية لسوق الغلوبولين المناعي الوريدي.
- يجب على الموزعين الحفاظ على مستوى من مخزون الأمان لضمان استمرارية الرعاية للمرضى الذين يعانون من ضعف المناعة والذين يحتاجون إلى علاج الغلوبولين المناعي كل 21-28 يومًا.
- يقوم موزعو شركة ADMA وعملاؤها المباشرون عادةً بتخزين كميات تتجاوز الحد الأدنى المطلوب بموجب العقد لضمان وجود إمدادات جاهزة للإدارة الفورية وللتخفيف من أي اضطرابات محتملة في سلسلة التوريد أو التصنيع أو الاختبار أو التنظيم.
- يقوم موزعو الشركة بتزويد شركة ADMA ببيانات المخزون وبيانات المبيعات بشكل مستمر.
- كما يتضح من البيانات المُقدمة مباشرةً من شركاء التوزيع وعملاء ADMA، تُظهر الرسوم البيانية بعنوان "أيام تغطية مخزون الموزعين فوق مخزون الأمان" أنه اعتبارًا من 5 يناير 2026 و22 مارس 2026، بلغ متوسط المخزون المتاح 84 و48 يومًا على التوالي لـ ASCENIV، ومتوسط المخزون المتاح 87 و51 يومًا على التوالي لـ BIVIGAM، وهو ما يتجاوز الحد الأدنى المطلوب من الموزعين. وقد حُسبت هذه البيانات باستخدام معدل مبيعات كل موزع للشهر السابق، مما يدل على استمرار إقبال المستهلكين على منتجات الغلوبولين المناعي من ADMA. ملاحظة: نظرًا لتقويم نهاية العام وجداول التقارير الثابتة، فإن تاريخ 5 يناير 2026 هو أقرب تاريخ متاح للبيانات لتاريخ 31 ديسمبر 2025.
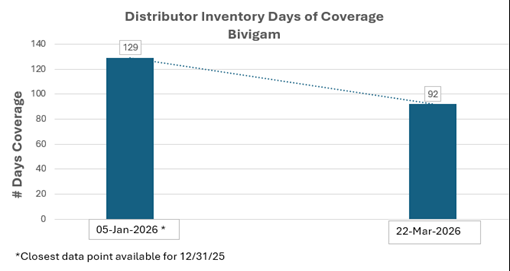
- كما هو موضح في البيانات المُقدمة مباشرةً من شركاء التوزيع وعملاء ADMA المباشرين، تُظهر الرسوم البيانية بعنوان "أيام تغطية مخزون الموزعين"، بتاريخ 5 يناير 2026 و22 مارس 2026، متوسط مخزون ASCENIV المتاح لمدة 128 و90 يومًا على التوالي، ومخزون BIVIGAM المتاح لمدة 129 و92 يومًا على التوالي، وذلك وفقًا لشركاء التوزيع وعملاء ADMA المباشرين، بما في ذلك مستويات مخزون الأمان المتفق عليها لمنتجات الغلوبولين المناعي من ADMA. ملاحظة: نظرًا لتقويم نهاية السنة وجداول إعداد التقارير الثابتة، فإن تاريخ 5 يناير 2026 هو أقرب تاريخ متاح للبيانات لتاريخ 31 ديسمبر 2025.
- وتعتقد الشركة أن مستويات المخزون هذه تتوافق مع نظرائها في الصناعة وأنها ذات حجم مناسب لضمان الشحن والتخزين والتعامل مع هذه المنتجات في سلسلة التبريد وللتخفيف من أي اضطرابات محتملة في سلسلة التوريد أو الإنتاج.



- يقدم التقرير الموجز معلومات مضللة ويخلط بين فائدة شركة ASCENIV وموقعها التنافسي في سوق IVIG.
- يتم وضع ASCENIV كعلاج متأخر للأفراد الذين يعانون من ضعف المناعة والذين لا يستجيبون لعلاجات الغلوبولين المناعي القياسية، ولديهم أمراض مصاحبة ويعانون من التهابات مزمنة ومستمرة.
- باعتباره علاجًا متأخرًا للمرضى الذين لم يستجيبوا للعلاج بالغلوبولين المناعي التقليدي، يُصنّف دواء ASCENIV ضمن فئة مختلفة، ولذا يُباع بسعر مرتفع. إن استشهاد التقرير الموجز بإطلاق منتجات جديدة من الغلوبولين المناعي كعامل مُحفز للمنافسة على استخدام ASCENIV هو استدلال خاطئ تمامًا.
- حصلت شركة ADMA على آراء غير مشروطة في عمليات التدقيق الخاصة بها للسنتين الماليتين 2024 و2025 .
- قدمت شركة ADMA تقاريرها السنوية على النموذج 10-K للسنوات المنتهية في 31 ديسمبر 2024 و2025 مع تقارير من إحدى شركات المحاسبة الأربع الكبرى التي أعربت عن آراء غير مشروطة بشأن فعالية الرقابة الداخلية للشركة على التقارير المالية وتقييم بأن البيانات المالية الموحدة للشركة معروضة بشكل عادل، من جميع النواحي الجوهرية، بما يتوافق مع مبادئ المحاسبة المقبولة عموماً في الولايات المتحدة (GAAP) لتلك الفترات.
- استقالت شركة المحاسبة السابقة للشركة في أواخر عام 2024 قبل أن تستحوذ عليها شركة أسهم خاصة.
- لم تُجرَ أي معاملات مع أطراف ذات صلة غير مُفصح عنها تُخالف قوانين الأوراق المالية الأمريكية. لم تقم أي جهة مملوكة أو خاضعة لسيطرة جيرولد غروسمان أو آدم غروسمان أو عائلة غروسمان بتوزيع أو امتلاك أو حيازة أي من منتجات الغلوبولين المناعي أو غيرها من منتجات ADMA، سواءً لإعادة البيع أو غيره. وتؤكد ADMA أنها لم تبع قط أيًا من منتجات الغلوبولين المناعي أو غيرها من المنتجات لأي جهة خاضعة لسيطرة عائلة غروسمان أو أي أطراف ذات صلة.
تلتزم شركة ADMA بقيادة عصر جديد في تصنيع وتسويق وتوزيع المنتجات البيولوجية المتخصصة للوقاية من الأمراض المعدية وعلاجها لدى المرضى ذوي المناعة الضعيفة وغيرهم من المرضى المعرضين لخطر الإصابة ببعض أنواع العدوى، وتحقيق قيمة طويلة الأجل لمساهميها. وللحصول على معلومات دقيقة حول الشركة، يُنصح جميع المستثمرين بمراجعة الوثائق التي قدمتها ADMA إلى هيئة الأوراق المالية والبورصات الأمريكية، والتي يمكن الوصول إليها أيضًا من خلال زيارة موقع الشركة الإلكتروني www.admabiologics.com .
نبذة عن ASCENIV™
أسينيف (غلوبولين مناعي وريدي بشري - سائل بتركيز 10%) هو غلوبولين مناعي وريدي متعدد النسائل مشتق من البلازما. حصل أسينيف على موافقة إدارة الغذاء والدواء الأمريكية (FDA) في أبريل 2019، ويُستخدم لعلاج نقص المناعة الخلطية الأولي (PI)، المعروف أيضًا باسم مرض نقص المناعة الأولي (PIDD)، لدى البالغين والمراهقين (من 12 إلى 17 عامًا). يُصنّع أسينيف باستخدام منهجية فحص متبرعي البلازما الفريدة والمُسجّلة ببراءة اختراع من قِبل شركة ADMA، وتصميم تجميع البلازما المُخصّص، والذي يمزج بلازما من مصدر طبيعي وبلازما فيروس الجهاز التنفسي المخلوي (RSV) المُستخلصة من متبرعين تم اختبارهم باستخدام فحص التحييد المجهري الخاص بالشركة. يحتوي أسينيف على أجسام مضادة متعددة النسائل طبيعية، وهي بروتينات يستخدمها جهاز المناعة في الجسم لتحييد الميكروبات مثل البكتيريا والفيروسات، مما يحمي من العدوى والأمراض. تتمتع شركة ASCENIV بحماية العديد من براءات الاختراع الصادرة في الولايات المتحدة وعلى الصعيد الدولي، بالإضافة إلى مجموعة واسعة من طلبات براءات الاختراع في جميع أنحاء العالم. يمكنكم الاطلاع على بعض البيانات والمعلومات الأخرى المتعلقة بشركة ASCENIV من خلال زيارة الموقع الإلكتروني www.asceniv.com . كما يمكنكم الاطلاع على معلومات حول شركة ADMA ومنتجاتها على موقعها الإلكتروني www.admabiologics.com .
معلومات أمان إضافية هامة حول ASCENIV™
| تحذير: تجلط الدم، خلل في وظائف الكلى، وفشل كلوي حاد |
| قد يحدث تجلط الدم مع منتجات الغلوبولين المناعي الوريدي (IGIV)، بما في ذلك ASCENIV. قد تشمل عوامل الخطر ما يلي: التقدم في السن، والجمود لفترات طويلة، وحالات فرط التخثر، وتاريخ الإصابة بتجلط الأوردة أو الشرايين، واستخدام الإستروجينات، والقسطرة الوعائية الدائمة، وفرط اللزوجة، وعوامل خطر الإصابة بأمراض القلب والأوعية الدموية. قد تحدث اختلالات في وظائف الكلى، وفشل كلوي حاد، واعتلال كلوي تناضحي، والوفاة مع إعطاء منتجات الغلوبولين المناعي الوريدي للمرضى المعرضين للخطر. يُعدّ خلل وظائف الكلى والفشل الكلوي الحاد أكثر شيوعًا لدى المرضى الذين يتلقون منتجات الغلوبولين المناعي الوريدي التي تحتوي على السكروز. أما دواء أسينيف فلا يحتوي على السكروز. بالنسبة للمرضى المعرضين لخطر الإصابة بالجلطات الدموية، أو خلل وظائف الكلى، أو الفشل الكلوي، يُعطى دواء أسينيف بأقل جرعة وأسرع معدل تسريب ممكن. يجب التأكد من ترطيب الجسم بشكل كافٍ قبل إعطاء الدواء. راقب ظهور علامات وأعراض الجلطات الدموية، وقيم لزوجة الدم لدى المرضى المعرضين لخطر فرط اللزوجة. |
موانع استخدام ASCENIV™:
تاريخ من ردود الفعل التحسسية المفرطة أو ردود الفعل الجهازية الشديدة تجاه الغلوبولين المناعي البشري.
المرضى الذين يعانون من نقص IgA ولديهم أجسام مضادة لـ IgA وتاريخ من فرط الحساسية.
تحذيرات واحتياطات ASCENIV™:
يُعدّ المرضى الذين يعانون من نقص IgA ولديهم أجسام مضادة ضد IgA أكثر عرضةً للإصابة بتفاعلات فرط حساسية شديدة وتفاعلات تأقية. لذا، يجب توفير أدوية مثل الإبينفرين لعلاج أي تفاعلات فرط حساسية حادة وشديدة. [4، 5.1]
حدثت جلطات دموية لدى المرضى الذين يتلقون علاجات الغلوبولين المناعي الوريدي. يجب مراقبة المرضى الذين لديهم عوامل خطر معروفة لحدوث الجلطات الدموية؛ وينبغي النظر في إجراء تقييم أساسي للزوجة الدم للمرضى المعرضين لخطر فرط اللزوجة. [5.2، 5.4]
في المرضى المعرضين لخطر الإصابة بالفشل الكلوي الحاد، يجب مراقبة وظائف الكلى، بما في ذلك نيتروجين اليوريا في الدم (BUN)، والكرياتينين في المصل، وكمية البول. [5.3، 5.9]
يمكن أن تحدث فرط بروتينات الدم، وزيادة لزوجة المصل، ونقص صوديوم الدم أو نقص صوديوم الدم الكاذب لدى المرضى الذين يتلقون علاج IGIV.
تم الإبلاغ عن متلازمة التهاب السحايا العقيم (AMS) مع علاجات IGIV، وخاصة مع الجرعات العالية أو التسريب السريع. [5.5]
قد يحدث فقر الدم الانحلالي بعد العلاج بالغلوبولين المناعي الوريدي. يجب مراقبة المرضى تحسباً لانحلال الدم وفقر الدم الانحلالي. [5.6]
يجب مراقبة المرضى تحسباً لحدوث تفاعلات رئوية ضائرة (إصابة الرئة الحادة المرتبطة بنقل الدم [TRALI]). في حال الاشتباه بإصابة الرئة الحادة المرتبطة بنقل الدم، يجب فحص المنتج والمريض للكشف عن الأجسام المضادة للعدلات. [5.7]
لأن هذا المنتج مصنوع من دم الإنسان، فقد يحمل خطر نقل العوامل المعدية، مثل الفيروسات، ونظريًا، عامل مرض كروتزفيلد جاكوب (CJD).
الآثار الجانبية لدواء ASCENIV™:
كانت أكثر ردود الفعل السلبية شيوعًا تجاه ASCENIV (≥5% من المشاركين في الدراسة) هي الصداع، والتهاب الجيوب الأنفية، والإسهال، والتهاب المعدة والأمعاء الفيروسي، والتهاب البلعوم الأنفي، وعدوى الجهاز التنفسي العلوي، والتهاب الشعب الهوائية، والغثيان.
للإبلاغ عن ردود الفعل السلبية المشتبه بها، اتصل بشركة ADMA Biologics على الرقم (800) 458-4244 أو إدارة الغذاء والدواء على الرقم 1-800-FDA-1088 أو www.fda.gov/medwatch .
نبذة عن BIVIGAM ®
بيفيجام (الغلوبولين المناعي الوريدي البشري - 10% سائل) هو غلوبولين مناعي وريدي متعدد النسائل مشتق من البلازما. تمت الموافقة على بيفيجام من قِبل إدارة الغذاء والدواء الأمريكية في مايو 2019، وهو مُخصص لعلاج نقص المناعة الخلطية الأولي، بما في ذلك، على سبيل المثال لا الحصر، مجموعة الاضطرابات الوراثية التالية: نقص غاما غلوبولين الدم المرتبط بالكروموسوم X ونقص غاما غلوبولين الدم الخلقي، ونقص المناعة المتغير الشائع، ومتلازمة ويسكوت-ألدريتش، ونقص المناعة المركب الشديد. يحتوي بيفيجام على مجموعة واسعة من الأجسام المضادة المشابهة لتلك الموجودة في بلازما الدم البشري الطبيعية. تستهدف هذه الأجسام المضادة البكتيريا والفيروسات، وتساعد على حماية مرضى نقص المناعة الخلطية الأولي من العدوى الخطيرة. بيفيجام عبارة عن مُستحضر مُنقّى ومعقم وجاهز للاستخدام من أجسام مضادة مركزة من الغلوبولين المناعي البشري. يمكن العثور على بيانات ومعلومات معينة حول BIVIGAM ® أو ADMA Biologics ومنتجاتها على موقع الشركة الإلكتروني www.admabiologics.com .
معلومات أمان إضافية هامة حول BIVIGAM ®
| تحذير: تجلط الدم، خلل في وظائف الكلى، وفشل كلوي حاد |
| قد تحدث الجلطات الدموية مع منتجات الغلوبولين المناعي الوريدي (IGIV)، بما في ذلك بيفيغام. تشمل عوامل الخطر ما يلي: التقدم في السن، وقلة الحركة لفترات طويلة، وحالات فرط التخثر، وتاريخ الإصابة بالجلطات الوريدية أو الشريانية، واستخدام الإستروجينات، والقسطرة الوعائية الدائمة، وفرط اللزوجة، وعوامل خطر الإصابة بأمراض القلب والأوعية الدموية. قد تحدث اختلالات في وظائف الكلى، وفشل كلوي حاد، واعتلال كلوي تناضحي، والوفاة مع إعطاء منتجات الغلوبولين المناعي الوريدي (البشري) (IGIV) للمرضى المعرضين لذلك. يُعدّ خلل وظائف الكلى والفشل الكلوي الحاد أكثر شيوعًا لدى المرضى الذين يتلقون منتجات الغلوبولين المناعي الوريدي التي تحتوي على السكروز. لا يحتوي دواء بيفيجام على السكروز. بالنسبة للمرضى المعرضين لخطر الإصابة بالجلطات الدموية، أو خلل وظائف الكلى، أو الفشل الكلوي، يُعطى دواء بيفيغام بأقل جرعة وأسرع معدل تسريب ممكن. يجب التأكد من ترطيب الجسم بشكل كافٍ قبل إعطاء الدواء. راقب ظهور علامات وأعراض الجلطات الدموية، وقيم لزوجة الدم لدى المرضى المعرضين لخطر فرط اللزوجة. |
موانع استخدام بيفيجام ® :
تاريخ من ردود الفعل التحسسية المفرطة أو ردود الفعل الجهازية الشديدة تجاه الغلوبولين المناعي البشري.
المرضى الذين يعانون من نقص IgA ولديهم أجسام مضادة لـ IgA وتاريخ من فرط الحساسية.
تحذيرات واحتياطات BIVIGAM ® :
حدثت جلطات دموية لدى المرضى الذين يتلقون العلاج بالغلوبولين المناعي الوريدي. يجب مراقبة المرضى الذين لديهم عوامل خطر معروفة لحدوث الجلطات الدموية؛ وينبغي النظر في إجراء تقييم أساسي للزوجة الدم لدى أولئك المعرضين لخطر فرط اللزوجة.
يُعدّ المرضى الذين يعانون من نقص IgA ولديهم أجسام مضادة ضد IgA أكثر عرضةً للإصابة بتفاعلات فرط حساسية شديدة وتفاعلات تأقية. لذا، يجب توفير أدوية مثل الإبينفرين فورًا لعلاج أي تفاعلات فرط حساسية حادة وشديدة.
مراقبة وظائف الكلى، بما في ذلك نيتروجين اليوريا في الدم (BUN) والكرياتينين في الدم، وكمية البول لدى المرضى المعرضين لخطر الإصابة بالفشل الكلوي الحاد.
يمكن أن تحدث فرط بروتينات الدم، وزيادة لزوجة المصل، ونقص صوديوم الدم أو نقص صوديوم الدم الكاذب لدى المرضى الذين يتلقون العلاج بالغلوبولين المناعي الوريدي.
تم الإبلاغ عن متلازمة التهاب السحايا العقيم (AMS) مع علاجات IGIV، وخاصة مع الجرعات العالية أو التسريب السريع.
قد يحدث فقر الدم الانحلالي بعد العلاج بمنتجات الغلوبولين المناعي الوريدي. يجب مراقبة المرضى تحسباً لانحلال الدم وفقر الدم الانحلالي.
يجب مراقبة المرضى تحسباً لحدوث تفاعلات رئوية ضائرة (إصابة الرئة الحادة المرتبطة بنقل الدم). في حال الاشتباه بإصابة الرئة الحادة المرتبطة بنقل الدم، يجب فحص المنتج والمريض للكشف عن الأجسام المضادة للعدلات.
لأن هذا المنتج مصنوع من دم الإنسان، فقد يحمل خطر نقل العوامل المعدية، مثل الفيروسات، ونظريًا، عامل مرض كروتزفيلد جاكوب (CJD).
الآثار الجانبية لدواء بيفيجام ® :
كانت أكثر ردود الفعل السلبية شيوعًا تجاه BIVIGAM (التي تم الإبلاغ عنها في ≥5٪ من المشاركين في الدراسة السريرية) هي الصداع والتعب وتفاعل موقع التسريب والغثيان والتهاب الجيوب الأنفية وارتفاع ضغط الدم والإسهال والدوخة والخمول.
للإبلاغ عن ردود الفعل السلبية المشتبه بها، يرجى الاتصال بشركة ADMA Biologics على الرقم (800) 458-4244 أو إدارة الغذاء والدواء على الرقم 1-800-FDA-1088 أو www.fda.gov/medwatch .
نبذة عن شركة ADMA Biologics, Inc. (ADMA)
شركة ADMA Biologics هي شركة أمريكية متكاملة في مجال المستحضرات الصيدلانية الحيوية، متخصصة في تصنيع وتسويق وتطوير منتجات بيولوجية متخصصة لعلاج المرضى الذين يعانون من نقص المناعة والمعرضين لخطر الإصابة بالعدوى، بالإضافة إلى علاج المرضى المعرضين لخطر الإصابة بأمراض معدية معينة. وتقوم ADMA حاليًا بتصنيع وتسويق ثلاثة منتجات بيولوجية مشتقة من البلازما، معتمدة من إدارة الغذاء والدواء الأمريكية (FDA)، لعلاج نقص المناعة والوقاية من بعض الأمراض المعدية: ASCENIV™ (غلوبولين مناعي وريدي بشري - سائل بتركيز 10%) لعلاج نقص المناعة الخلطية الأولي؛ وBIVIGAM® (غلوبولين مناعي وريدي بشري) لعلاج نقص المناعة الخلطية الأولي؛ وNABI- HB® (غلوبولين مناعي بشري لالتهاب الكبد B) لتعزيز المناعة ضد فيروس التهاب الكبد B. إضافةً إلى ذلك، تعمل ADMA على تطوير SG-001، وهو غلوبولين مناعي فائق في مرحلة ما قبل التجارب السريرية، يستهدف بكتيريا المكورات الرئوية . تُصنّع شركة ADMA منتجاتها من الغلوبولين المناعي، بالإضافة إلى المنتجات المرشحة، في منشأة تجزئة وتنقية البلازما التابعة لها والمرخصة من قِبل إدارة الغذاء والدواء الأمريكية، والواقعة في بوكا راتون، فلوريدا. كما تعمل ADMA، من خلال شركتها التابعة ADMA BioCenters، كمصدر معتمد من إدارة الغذاء والدواء الأمريكية لجمع بلازما الدم في الولايات المتحدة، حيث تُزوّدها ببلازما الدم اللازمة لتصنيع منتجاتها ومنتجاتها المرشحة. وتتمثل مهمة ADMA في تصنيع وتسويق وتطوير أنواع متخصصة من الغلوبولين المناعي البشري المشتق من البلازما، والموجهة لفئات محددة من المرضى، وذلك لعلاج والوقاية من بعض الأمراض المعدية، وإدارة حالات المرضى الذين يعانون من نقص المناعة، سواءً كان ذلك بسبب نقص مناعي كامن أو لأسباب طبية أخرى. تمتلك ADMA العديد من براءات الاختراع الأمريكية والأجنبية المتعلقة بمنتجاتها ومنتجاتها المرشحة، والتي تشمل جوانب مختلفة منها. لمزيد من المعلومات، يُرجى زيارة الموقع الإلكتروني www.admabiologics.com .
ملاحظة تحذيرية بشأن البيانات التطلعية
يحتوي هذا البيان الصحفي على "بيانات تطلعية" وفقًا لأحكام الملاذ الآمن لقانون إصلاح التقاضي بشأن الأوراق المالية الخاصة لعام 1995، بشأن شركة ADMA Biologics, Inc. ("نحن" أو "شركتنا"). تشمل البيانات التطلعية، على سبيل المثال لا الحصر، أي بيان قد يتنبأ أو يتوقع أو يشير أو يلمح إلى نتائج أو أداء أو إنجازات مستقبلية، وقد يحتوي على كلمات مثل "واثقون" و"نقدر" و"نتوقع" و"ننوي" و"نتنبأ" و"نستهدف" و"نتوقع" و"نخطط" و"نتوقع" و"نعتقد" و"سوف" و"من المرجح" و"من المرجح أن" و"نضع أنفسنا" و"مؤهلون" و"ندعم" و"ينبغي" و"يمكن" و"قد" و"إمكانية" و"فرصة"، أو في كل حالة، نفيها، أو كلمات أو تعابير ذات معنى مماثل. تشمل هذه البيانات التطلعية، على سبيل المثال لا الحصر، بيانات حول شركة شورت ريبورت، بما في ذلك مستويات مخزون الشركة وعدد أيام التوافر واستخدام المنتج. قد تختلف الأحداث أو النتائج الفعلية اختلافًا جوهريًا عن تلك المذكورة في هذا البيان الصحفي نظرًا لعدد من العوامل المهمة. يُنصح حاملو الأوراق المالية الحاليون والمحتملون بأنه لا يوجد ما يضمن دقة البيانات التطلعية الواردة في هذا البيان الصحفي. باستثناء ما يقتضيه القانون أو اللوائح المعمول بها، لا تلتزم شركة ADMA بتحديث أي بيانات تطلعية أو الإعلان عن أي تعديلات عليها. تخضع البيانات التطلعية للعديد من المخاطر والشكوك والعوامل الأخرى التي قد تؤدي إلى اختلاف نتائجنا الفعلية، وتوقيت بعض الأحداث، اختلافًا جوهريًا عن أي نتائج مستقبلية صريحة أو ضمنية في هذه البيانات، بما في ذلك، على سبيل المثال لا الحصر، المخاطر والشكوك المذكورة في ملفاتنا لدى هيئة الأوراق المالية والبورصات الأمريكية، بما في ذلك أحدث تقاريرنا على النماذج 10-K و10-Q و8-K، وأي تعديلات عليها.
للتواصل مع قسم علاقات المستثمرين:
أرجوت بارتنرز | 212-600-1902 | ADMA@argotpartners.com
للتواصل الإعلامي:
شركاء لونغ آكر سكوير | ADMABiologics@longacresquare.com
تتوفر الصور المصاحبة لهذا الإعلان على الموقع الإلكتروني التالي:
https://www.globenewswire.com/NewsRoom/AttachmentNg/fa2ef727-67b9-47b9-8903-3327560f7723
https://www.globenewswire.com/NewsRoom/AttachmentNg/1c4170ed-8dfa-46dc-87d2-4dc69bd58671
https://www.globenewswire.com/NewsRoom/AttachmentNg/cc3886f3-76e6-4df6-a915-1e5106dad222
https://www.globenewswire.com/NewsRoom/AttachmentNg/52920050-f97e-4b6f-aaec-4234d158f7ce
https://www.globenewswire.com/NewsRoom/AttachmentNg/c2e4dfc0-94d2-4de6-8ca0-8e790ba8a1ee
