تعلن شركة بيوهافن عن نتائجها على مدى ثلاث سنوات في علاج ترنح المخيخ الشوكي
Biohaven Ltd. BHVN | 9.80 | +1.87% |
أعلنت شركة بيوهافن المحدودة (بورصة نيويورك: BHVN ) (أو بيوهافن أو الشركة) اليوم عن نتائج إيجابية من الدراسة المحورية BHV4157-206-RWE (NCT06529146) التي توضح فعالية التريلوزول في متوسط التغير من الأساس في f-SARA بعد 3 سنوات من العلاج. حققت الدراسة نقطة النهاية الأولية وأظهرت تحسنات ذات دلالة إحصائية في f-SARA في العامين الأول والثاني (الشكل 1). SCA هو مرض تنكسي عصبي نادر وموهن تدريجيًا يصيب حوالي 15000 شخص في الولايات المتحدة و24000 في أوروبا والمملكة المتحدة. لا توجد علاجات معتمدة من إدارة الغذاء والدواء الأمريكية لـ SCA.
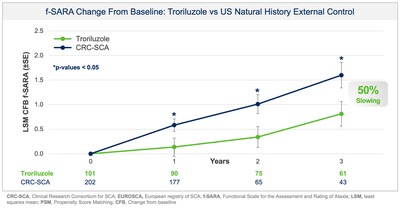
بشكل جماعي، توضح البيانات عبر تحليلات متعددة تباطؤًا قويًا وذو مغزى سريريًا لتقدم المرض لدى مرضى SCA. تترجم فوائد العلاج هذه إلى معدل انحدار أبطأ بنسبة 50-70% مقارنة بالمرضى غير المعالجين، وهو ما يمثل تأخيرًا لمدة 1.5-2.2 سنة في تقدم المرض خلال فترة الدراسة التي استمرت 3 سنوات. بالإضافة إلى ذلك، في تحليل حساسية المستجيب، أظهر تقدم المرض عند تعريفه بتدهور بمقدار 2 نقطة أو أكثر على f-SARA بعد 3 سنوات نسبة احتمالات (OR) تبلغ 4.1 (95% CI: 2.1، 8.1) للذراع التحكمي الخارجي غير المعالج مقابل الأشخاص المعالجين بالترويلوزول (p < 0.0001؛ تحليل مجمع).
صرحت الدكتورة سوزان بيرلمان، مديرة عيادة الرنح والتجارب السريرية لعلم الأعصاب الجيني في كلية ديفيد جيفن للطب بجامعة كاليفورنيا في لوس أنجلوس، قائلة: "إن SCA هو مرض منهك ومتقدم بلا هوادة يدمر جودة الحياة، ويجعل المرضى غير قادرين على رعاية أنفسهم أو المشي أو التحدث. يعد عقار ترويلوزول أول علاج يظهر تأخيرًا في تقدم المرض مما قد يمنح المرضى سنوات إضافية من الاستقلال، حيث يمكنهم المشي دون مساعدة، ومواصلة العمل، واللعب مع أطفالهم، والمشاركة في الأنشطة اليومية. هذه لحظة مثيرة ومليئة بالأمل لمجتمع SCA".
صُممت الدراسة BHV4157-206-RWE، بالتشاور مع إدارة الغذاء والدواء الأمريكية (FDA)، لتقييم فعالية التريلوزول في SCA بعد 3 سنوات من العلاج كما تم قياسه من خلال التغيير من الأساس في f-SARA. استخدمت الدراسة بيانات المرحلة 3 وتحكمًا خارجيًا لمرضى SCA المطابقين وغير المعالجين من اتحاد الأبحاث السريرية الأمريكي لدراسة ترنح المخيخ (CRC-SCA) وفقًا لإرشادات إدارة الغذاء والدواء بشأن الأدلة الواقعية (RWE) للفعالية. تم تحديد جميع نقاط النهاية مسبقًا، وتم تقديم كل من بروتوكول الدراسة وخطة التحليل الإحصائي إلى إدارة الغذاء والدواء الأمريكية ومراجعتها قبل تحليل البيانات الأولية. ضاعف التحليل الجديد بيانات السنوات الثلاث المتاحة سابقًا مع 63 مريضًا أكملوا الآن 3 سنوات من العلاج بالتريلوزول ومطابقين لذراع التحكم الخارجية. تم استخدام مطابقة درجات الميل (PSM) لضمان مطابقة المرضى غير المعالجين من دراسة CRC-SCA بدقة مع المرضى المعالجين من الدراسة BHV4157-206 على الخصائص الأساسية. كان الهدف الأساسي هو فحص تأثيرات العلاج بالترويلوزول لمدة تصل إلى 3 سنوات، من خلال مقارنة البيانات على f-SARA من المرضى المعالجين بالترويلوزول في الدراسة BHV4157-206 بالمرضى غير المعالجين من دراسة التاريخ الطبيعي. أظهر المرضى المعالجون بالترويلوزول فوائد ذات دلالة إحصائية ومستدامة في السنوات 1 و2 و3 على f-SARA مقارنة بمجموعة تحكم التاريخ الطبيعي المطابقة بدقة.
بالإضافة إلى ذلك، استخدمت التحليلات المحددة مسبقًا في البروتوكول عنصر تحكم تاريخي طبيعي منفصل ومستقل عن دراسة التاريخ الطبيعي الأوروبية SCA (EUROSCA) لأغراض تنظيمية عالمية. كانت النتائج باستخدام مرضى EUROSCA، بالإضافة إلى تحليل مجمع باستخدام كل من مرضى CRC-SCA وEUROSCA، كعناصر تحكم خارجية، ذات دلالة إحصائية ومتسقة مع تحليل الفعالية الأساسي في جميع النقاط الزمنية (انظر الشكل 2 والشكل 3). أدت إضافة بيانات EUROSCA إلى زيادة حجم عينة التحكم الخارجية وإضافة إلى قوة الاختلافات العلاجية ذات الدلالة الإحصائية في السنوات 1 و2 و3، لصالح ترويلوزول.
علق الدكتور جيريمي شمهمان، أستاذ علم الأعصاب في كلية الطب بجامعة هارفارد والمدير المؤسس لمركز أتاكسيا في مستشفى ماساتشوستس العام، قائلاً: "إن استقرار أعراض SCA كما تعكسه البيانات الأولية بعد 3 سنوات إلى جانب الانخفاضات المبلغ عنها سابقًا في حالات السقوط تظهر الإمكانات العلاجية للترويلوزول. لا أستطيع أن أؤكد بما فيه الكفاية على تأثير العلاج المحتمل الذي يمكن أن يبطئ تقدم مرض SCA وتأثيره على المرضى ومقدمي الرعاية الذين شاهدوا أجيالًا من أفراد الأسرة يتدهورون ويموتون بسبب SCA. توفر هذه البيانات الجديدة الدعم للترويلوزول كعلاج آمن وفعال مرة واحدة يوميًا لمرضى SCA."
خلل التنسج المخيخي الشوكي هو مجموعة من الاضطرابات العصبية التنكسية الوراثية السائدة التي تتميز بفقدان تدريجي للتحكم الحركي الطوعي وضمور المخيخ وجذع الدماغ والحبل الشوكي. يعاني المرضى من اعتلالات مرضية كبيرة، بما في ذلك التقدم إلى كرسي متحرك، واضطراب في المشي يؤدي إلى السقوط، وعدم القدرة على التواصل بسبب ضعف الكلام، وصعوبة البلع، والوفاة المبكرة. في حين أن العلامات والأعراض يمكن أن تظهر في أي وقت من الطفولة إلى أواخر مرحلة البلوغ، فإن SCA يظهر عادةً في أوائل مرحلة البلوغ ويتطور على مدى عدد من السنوات. حاليًا، لا توجد علاجات معتمدة من إدارة الغذاء والدواء الأمريكية ولا يوجد علاج لـ SCA.
صرح الدكتور فلاد كوريك، الرئيس التنفيذي ورئيس مجلس إدارة شركة بيوهافن، قائلاً: "إن تطوير علاجات جديدة للمرضى المصابين بأمراض نادرة غالبًا ما يكون عملية تستغرق سنوات عديدة من التعاون بين الشركاء الأكاديميين ومناصري المرضى والجهات التنظيمية والصناعية. لطالما التزم فريق بيوهافن باتباع العلم بدقة في هذا المجال، ومن خلال شراكتنا مع مؤسسة National Ataxia Foundation والتعاون مع كبار خبراء SCA في جميع أنحاء العالم، قدم برنامج تطوير SCA لدينا أول دليل على فائدة علاجية ذات مغزى سريري بالإضافة إلى إبطاء تقدم المرض لدى مرضى SCA. لقد كنا متحمسين لتلقي النتائج الإيجابية من الدراسة BHV4157-206-RWE، والتي تم تصميمها بمدخلات من إدارة الغذاء والدواء ووفقًا للمبادئ الموضحة في إرشادات إدارة الغذاء والدواء لاستخدام الأدلة الواقعية. إن الحاجة إلى علاجات لهذا المرض التنكسي العصبي المميت ملحة. كشركة، نظل ملتزمين بتطوير علاجات جديدة للمرضى الذين يعيشون باضطرابات نادرة بدون علاجات معتمدة، مثل SCA. ونحن نتطلع إلى التفاعل مع الهيئات التنظيمية لتوفير عقار ترويلوزول للمرضى الذين يعانون من SCA.
صرح أندرو روزن، الرئيس التنفيذي لمؤسسة الرنح الوطني (NAF)، قائلاً: "كانت شركة Biohaven أول شركة تنضم إلى مجموعة تطوير الأدوية التابعة لمؤسسة NAF (DDC)، وهي مجموعة من شركات الأدوية المخصصة لجمع المدافعين والأطباء والهيئات التنظيمية ومجتمع المرضى لتطوير الأبحاث وتسهيل تطوير علاجات الرنح. إن النتائج الرئيسية اليوم هي تتويج لسنوات مخصصة لدراسة التريلوزول كعلاج لمرض SCA. لقد كان المرضى والأسر ينتظرون لعقود من الزمن علاجًا يمكن أن يبطئ تقدم المرض في هذا الاضطراب المدمر والمتقدم بلا هوادة".
استنادًا إلى البيانات الأولية من دراسة BHV4157-206-RWE، وبيانات السلامة والفعالية السابقة من برنامج تطوير التريلوزول في SCA، تخطط Biohaven لتقديم طلب دواء جديد (NDA) إلى إدارة الغذاء والدواء في الربع الرابع من عام 2024. وقد أنتج برنامج تطوير التريلوزول أكبر مجموعة بيانات للتجارب السريرية في SCA ولديه الآن متابعة لبعض المرضى الذين عولجوا بالتريلوزول لأكثر من 5 سنوات. تلقت Biohaven سابقًا كل من تصنيف Fast-Track وOrphan drug (ODD) من إدارة الغذاء والدواء، وODD من وكالة الأدوية الأوروبية، للتريلوزول في SCA. إن طلب NDA مع ODD مؤهل لمراجعة FDA الأولية. ستكون Biohaven مستعدة لتسويق SCA في الولايات المتحدة في عام 2025، إذا تمت الموافقة عليه في النهاية، بناءً على جداول زمنية محتملة لمراجعة الأولوية.
