حصلت شركة BriaCell على موافقة إدارة الغذاء والدواء الأمريكية لبدء الدراسة السريرية Bria-BRES+™ لعلاج سرطان الثدي
BriaCell Therapeutics Corp Warrant 2021-26.02.26 on BriaCell Therapeutics BCTXW | 0.00 | |
BriaCell Therapeutics Corp Warrant - on BriaCell Therapeutics BCTXZ | 0.00 | |
BriaCell Therapeutics Corp Warrant 2026-15.01.31 On BriaCell Therap BCTXL | 0.00 | |
BriaCell Therapeutics Corp BCTX | 0.00 |
- موافقة إدارة الغذاء والدواء الأمريكية على طلب دواء تجريبي جديد (IND) تمهد الطريق لبدء المرحلة الأولى/الثانية من الدراسة السريرية لعقار بريا-بريس+ لعلاج سرطان الثدي النقيلي
- يُعدّ Bria-BRES+ الجيل التالي من العلاج المناعي الشخصي لسرطان الثدي من شركة BriaCell، ويتميز بمكونات إضافية لتنشيط المناعة مصممة لتعزيز الفعالية السريرية.
- قامت شركة بريا سيل بتجهيز الإمدادات السريرية من بريا-بريس+ وتخطط لبدء دراسة سريرية من المرحلة الأولى/الثانية لعلاج سرطان الثدي النقيلي في الأشهر المقبلة
فيلادلفيا وفانكوفر، كولومبيا البريطانية، 6 مايو 2026 (جلوب نيوزواير) - يسر شركة برياسيل ثيرابيوتكس (ناسداك: BCTX، BCTXL) (بورصة تورنتو: BCT) ("برياسيل" أو "الشركة")، وهي شركة للتكنولوجيا الحيوية في المرحلة السريرية تعمل على تطوير علاجات مناعية جديدة لتحويل رعاية مرضى السرطان، أن تعلن أنها حصلت على موافقة إدارة الغذاء والدواء لبدء التقييم السريري لـ Bria-BRES+، وهو الجيل التالي من العلاج المناعي الخلوي الشخصي والجاهز للاستخدام لعلاج سرطان الثدي النقيلي.
صرح الدكتور ويليام ف. ويليامز، الرئيس والمدير التنفيذي لشركة بريا سيل: "يشرفنا الإعلان عن حصول أول طلب دواء جديد (IND) من إدارة الغذاء والدواء الأمريكية (FDA) لعلاجنا المناعي الشخصي من الجيل التالي، بريا-بريس+. يتميز بريا-بريس+ بتصميمه الفريد الذي يوفر إمكانية تحقيق مستوى أمان عالٍ وفائدة علاجية ملموسة في حالات سرطان الثدي النقيلي. نتطلع إلى بدء التجارب السريرية على بريا-بريس+ سعيًا منا لمنح الأمل لهؤلاء المرضى الذين لا تتوفر لديهم سوى خيارات علاجية قليلة أو معدومة."
كما ورد في العرض التقديمي الأخير لشركة بريا سيل في المؤتمر السنوي للجمعية الأمريكية لأبحاث السرطان (AACR) حول التجارب السريرية قبل السريرية ، أظهر علاج بريا-بريس+ تنشيطًا لكلٍ من المناعة التكيفية والفطرية، بما في ذلك تنشيط الخلايا التائية الساذجة (الخاملة)، والخلايا المتغصنة، والخلايا القاتلة الطبيعية. وتعتقد بريا سيل أن هذا التنشيط المناعي متعدد الجوانب قد يُحسّن الفعالية السريرية ويساعد في منع إفلات الجهاز المناعي لدى المرضى المصابين بسرطان الثدي النقيلي.
يستند علاج Bria-BRES+ من شركة BriaCell إلى برنامجها السريري لعلاج سرطان الثدي Bria-OTS™، حيث شهدت أول مريضة تلقت العلاج شفاءً تامًا ومستدامًا من ورم خبيث في الرئة . وقد حققت هذه السيدة البالغة من العمر 78 عامًا، والمصابة بسرطان الثدي النقيلي المتقدم والتي عانت من فشل علاجات سابقة متعددة، شفاءً تامًا (100%) من ورم خبيث في الرئة بعد أربع جرعات من العلاج الأحادي بـ Bria-OTS. وقد تأكدت الاستجابة الكاملة للورم، التي لوحظت مبدئيًا بعد شهرين، بعد أربعة أشهر، وستة أشهر، وأحد عشر شهرًا. تلقت المريضة 17 دورة علاجية من Bria-OTS، وأكملت 12 شهرًا من الدراسة، وما زالت تخضع للمتابعة الطبية.
الشكل 1: كما ورد سابقًا في يناير 2026، أدى العلاج باستخدام العلاج الأحادي Bria-OTS إلى زوال الورم بنسبة 100٪ في الرئة اليمنى لمريض سرطان الثدي النقيلي (MBC) بعد شهرين من العلاج وتم تأكيد ذلك في 4 و 6 و 11 شهرًا من العلاج 1 (مناظر محورية وإكليلية).
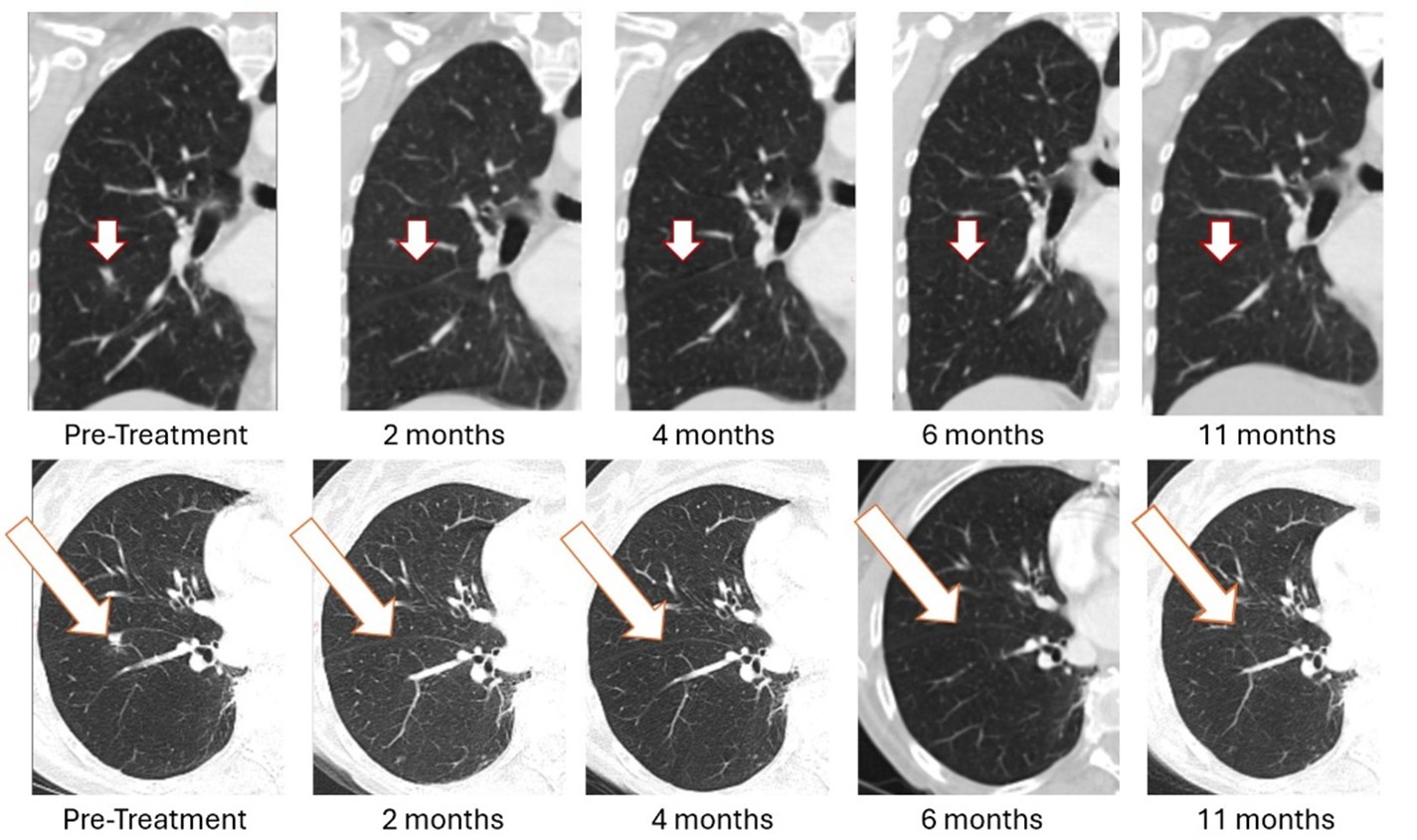
1 لاحظ أن النقاط البيضاء الأخرى في الرئتين هي أوعية دموية.
نبذة عن شركة بريا سيل ثيرابيوتكس
شركة بريا سيل هي شركة للتكنولوجيا الحيوية متخصصة في علم المناعة السرطانية، تعمل على تطوير أساليب علاجية فعّالة وموجهة لإدارة السرطان. للمزيد من المعلومات، تفضلوا بزيارة الموقع الإلكتروني https://briacell.com/ .
الملاذ الآمن
يحتوي هذا البيان الصحفي على "بيانات استشرافية" تخضع لمخاطر وشكوك كبيرة. جميع البيانات الواردة في هذا البيان الصحفي، باستثناء البيانات المتعلقة بالحقائق التاريخية، هي بيانات استشرافية. يمكن تحديد البيانات الاستشرافية الواردة في هذا البيان الصحفي من خلال استخدام كلمات مثل "نتوقع"، "نعتقد"، "نفكر"، "يمكن"، "نقدر"، "نأمل"، "ننوي"، "نسعى"، "قد"، "ربما"، "نخطط"، "إمكانية"، "نتنبأ"، "نتوقع"، "نستهدف"، "نهدف"، "ينبغي"، "سوف"، "قد"، أو نفي هذه الكلمات أو تعابير أخرى مماثلة، مع العلم أن ليس كل البيانات الاستشرافية تحتوي على هذه الكلمات. تستند البيانات التطلعية، بما في ذلك تلك المتعلقة بموافقة إدارة الغذاء والدواء الأمريكية على طلب دواء جديد قيد التحقيق (IND) والبدء المخطط له لدراسة سريرية من المرحلة الأولى/الثانية (أ) لـ Bria-BRES+، والتوقعات المتعلقة بالفوائد السريرية المحتملة لمنصة Bria-OTS+، إلى توقعات شركة BriaCell الحالية، وتخضع لشكوك ومخاطر وافتراضات كامنة يصعب التنبؤ بها. علاوة على ذلك، تستند بعض البيانات التطلعية إلى افتراضات بشأن أحداث مستقبلية قد لا تثبت صحتها. تُفصّل هذه المخاطر وغيرها من الشكوك تحت عنوان "المخاطر والشكوك" في أحدث تقرير للإدارة وتحليلها، وتحت عنوان "عوامل الخطر" في أحدث نموذج معلومات سنوي، وتحت عنوان "المخاطر والشكوك" في ملفات الشركة الأخرى لدى هيئات تنظيم الأوراق المالية الكندية وهيئة الأوراق المالية والبورصات الأمريكية، والتي يمكن الاطلاع عليها جميعًا في ملفات الشركة على نظام SEDAR+ على الموقع www.sedarplus.ca وعلى نظام EDGAR على الموقع www.sec.gov . وتُعتبر البيانات التطلعية الواردة في هذا الإعلان سارية اعتبارًا من هذا التاريخ، ولا تلتزم شركة BriaCell Therapeutics Corp. بتحديث هذه المعلومات إلا بما يقتضيه القانون المعمول به.
لا تتحمل بورصة تورنتو ولا مزود خدمات التنظيم التابع لها (كما هو محدد في سياسات بورصة تورنتو) المسؤولية عن كفاية أو دقة هذا البيان.
معلومات الاتصال
للتواصل مع الشركة:
ويليام ف. ويليامز، دكتور في الطب
الرئيس والمدير التنفيذي
1-888-485-6340
info@briacell.com
للتواصل مع قسم علاقات المستثمرين:
investors@briacell.com
تتوفر صورة مصاحبة لهذا الإعلان على الرابط التالي: https://www.globenewswire.com/NewsRoom/AttachmentNg/cf1af19a-fd92-49b4-8e39-fb9b1c4191a7

