النتائج الأولية للسنة المنتهية في 31 ديسمبر 2025
MIDATECH PHARMA PLC SPON ADS EACH REP 5 ORD BDRX | 0.00 |
27 مارس 2026
شركة بيوديكسا للأدوية بي إل سي
("Biodexa" أو "الشركة" أو، مع الشركات التابعة لها، "المجموعة")
النتائج الأولية للسنة المنتهية في 31 ديسمبر 2025
أعلنت شركة Biodexa Pharmaceuticals PLC (المدرجة في بورصة ناسداك تحت الرمز: BDRX)، وهي شركة أدوية بيولوجية في المرحلة السريرية تعمل على تطوير منتجات مبتكرة تركز على علاج أو الوقاية من سرطانات الجهاز الهضمي، عن نتائجها الأولية المدققة للسنة المنتهية في 31 ديسمبر 2025.
للمزيد من المعلومات، يرجى الاتصال على:
شركة بيوديكسا للأدوية بي إل سي
ستيفن ستامب، الرئيس التنفيذي
فيونا شارب، المدير المالي
الهاتف: +44 (0)29 2048 0180
www.biodexapharma.com
نبذة عن بيوديكسا
تشمل برامج التطوير الرئيسية للشركة eRapa، قيد التطوير لعلاج داء السلائل الورمي الغدي العائلي وسرطان المثانة غير الغازي للعضلات، وMTX240 قيد التطوير لعلاج أورام الجهاز الهضمي اللحمية (GIST)، وتوليميدون، قيد التطوير لعلاج مرض السكري من النوع 1.
إيرابا هو تركيبة كبسولات فموية مسجلة الملكية من الراباميسين، المعروف أيضاً باسم سيروليموس. الراباميسين هو مثبط لـ mTOR (الهدف الثديي للراباميسين). وقد ثبت أن لـ mTOR دوراً هاماً في مسار الإشارات الذي ينظم استقلاب الخلايا ونموها وتكاثرها، ويتم تنشيطه أثناء تكوين الأورام.
يُعدّ MTX240 بمثابة غراء جزيئي، حيث يجمع بروتينين داخل خلويين، هما PDE3a وSLFN12، واللذان تُعبّر عنهما خلايا سرطان الجهاز الهضمي اللحمي (GIST) بشكل مشترك، في مكان قريب لتشكيل مُركّب مستقر. يُثبّت هذا التفاعل بروتين SLFN12، مما يُمكّنه من تحفيز موت الخلايا المبرمج بوساطة RNase في خلايا GIST من خلال آلية مستقلة عن إشارات KIT.
توليميدون هو مثبط قوي وانتقائي لكيناز لين، يُعطى عن طريق الفم. لين هو أحد أفراد عائلة كينازات التيروزين البروتينية Src، والتي تُعبر عنها بشكل رئيسي الخلايا المكونة للدم، والأنسجة العصبية، والكبد، والأنسجة الدهنية. يُظهر توليميدون قدرة على التحكم في مستوى السكر في الدم عن طريق تحسين حساسية الأنسولين في النماذج الحيوانية لمرض السكري، ولديه القدرة على أن يصبح أول دواء من نوعه لتعديل مستوى السكر في الدم.
يقع المقر الرئيسي لشركة Biodexa ومرفق البحث والتطوير التابع لها في كارديف، المملكة المتحدة. لمزيد من المعلومات، تفضل بزيارة الموقع الإلكتروني www.biodexapharma.com .
البيانات التطلعية
قد تُعتبر بعض البيانات الواردة في هذا الإعلان "بيانات استشرافية" وفقًا للتشريعات المعمول بها في المملكة المتحدة و/أو الولايات المتحدة. وتُقدَّم هذه البيانات بموجب أحكام الملاذ الآمن لقانون إصلاح التقاضي في الأوراق المالية الخاصة لعام 1995، وهي تستند إلى اعتقاد الإدارة أو تفسيرها. يجب اعتبار جميع البيانات الواردة في هذا الإعلان، والتي لا تتعلق بوقائع تاريخية، بيانات استشرافية. في بعض الحالات، يمكن تحديد البيانات الاستشرافية من خلال استخدام كلمات مثل "يخطط" أو "يتوقع" أو "لا يتوقع" أو "يعتقد"، أو صيغ مختلفة من هذه الكلمات والعبارات، أو من خلال بيانات تفيد بأن إجراءات أو أحداثًا أو نتائج معينة "قد" أو "يمكن" أو "سوف" أو "من المحتمل" أن تُتخذ أو "تحدث" أو "تُحقق". تخضع البيانات والمعلومات التطلعية لمخاطر وشكوك مختلفة معروفة وغير معروفة، وكثير منها خارج عن قدرة الشركة على التحكم أو التنبؤ، والتي قد تتسبب في اختلاف نتائجها أو أدائها أو إنجازاتها الفعلية اختلافًا جوهريًا عن تلك المذكورة صراحة أو ضمنًا، ويتم تطويرها بناءً على افتراضات حول هذه المخاطر والشكوك والعوامل الأخرى الموضحة هنا.
يُرجى الرجوع إلى الوثائق التي ستقدمها شركة بيوديكسا من حين لآخر، أو الإعلانات التي قد تصدرها وفقًا للقواعد واللوائح الصادرة عن هيئة الأوراق المالية والبورصات الأمريكية، والتي تتضمن وتحدد عوامل أخرى مهمة قد تؤدي إلى اختلاف النتائج الفعلية اختلافًا جوهريًا عن تلك الواردة في أي توقعات أو بيانات استشرافية. وتُعتبر هذه البيانات الاستشرافية سارية فقط اعتبارًا من تاريخ هذا الإعلان. وتخضع جميع البيانات الاستشرافية اللاحقة، سواءً كانت مكتوبة أو شفهية، الصادرة عن شركة بيوديكسا أو المتعلقة بها، بشكل كامل للبيانات التحذيرية المذكورة أعلاه. وباستثناء ما قد يقتضيه القانون الأمريكي، لا تلتزم شركة بيوديكسا بتحديث أو مراجعة أي بيانات استشرافية علنًا بسبب معلومات جديدة أو أحداث مستقبلية أو أي أحداث أخرى قد تطرأ.
مقدمة
شركة Biodexa، التي يقع مقرها الرئيسي في كارديف بالمملكة المتحدة، هي شركة أدوية بيولوجية مدرجة في بورصة ناسداك، تعمل على تطوير منتجات مبتكرة تركز على علاج أو الوقاية من سرطانات الجهاز الهضمي بما في ذلك داء السلائل الورمي الغدي العائلي (FAP) وأورام اللحمة المعدية المعوية (GIST).
حتى العام الماضي، كانت الشركة تعمل على تطوير MTX110 لعلاج سرطانات الدماغ النادرة/اليتيمة، ولكن بسبب قيود الموارد، تم تخفيض أولوية هذه البرامج وإزالتها من خط أنابيب البحث والتطوير.
الاستراتيجية
اكتمل تحوّل الشركة من شركة متخصصة في توصيل الأدوية إلى شركة متخصصة في العلاجات ذات القيمة المضافة العالية في عام 2025. ومع حصولنا على ترخيص MTX240 من شركة أوتسوكا للأدوية المحدودة ("أوتسوكا") في فبراير 2026، يزداد تركيزنا في تطوير منتجاتنا على برامج أمراض الجهاز الهضمي والأورام. جميع منتجاتنا قيد التطوير في المرحلة السريرية، ونعتقد أنها توفر إمكانات كبيرة لتحسين نتائج علاج المرضى.
أولوياتنا لعام 2026 هي كالتالي:
| الضرورات الاستراتيجية | التقدم المحرز في عام 2025 | الأولويات لعام 2026 |
| تطوير مواردنا التنموية من خلال العيادة | أعلنا عن الإنجازات السريرية التالية في عام 2025: مارس : تعيين شركة Precision for Medicine كمنظمة أبحاث تعاقدية لإدارة الجزء الأوروبي من المرحلة الثالثة من تجربة Serenta مارس : اجتماع ناجح من النوع "ج" مع إدارة الغذاء والدواء الأمريكية، مما مهد الطريق لبدء المرحلة الثالثة من تجربة سيرينتا في الولايات المتحدة. يونيو : تسجيل أول مريض في دراسة المرحلة الثانية (أ) لعقار توليميدون في علاج داء السكري من النوع الأول من قبل معهد السكري بجامعة ألبرتا أغسطس: تسجيل أول مريض أمريكي في المرحلة الثالثة من تجربة سيرينتا نوفمبر: استلام موافقة وكالة الأدوية الأوروبية على طلب إجراء تجربة سريرية ديسمبر : تسجيل أول مريض أوروبي في المرحلة الثالثة من تجربة سيرينتا | تسريع عملية تجنيد المرضى في المرحلة الثالثة من تجربة سيرينتا لعقار إيرابا لعلاج مرضى داء السلائل الورمي الغدي العائلي في الولايات المتحدة وأوروبا وربما آسيا استمرار التواصل مع مجموعات دعم مرضى داء السلائل الورمي الغدي العائلي في الولايات المتحدة وأوروبا أكمل دراسة التوافر الحيوي لـ eRapa مقارنة بـ Rapamune® بدء دراسة المرحلة 1ب/2أ لتصعيد الجرعة وتوسيع نطاقها لعقار MTX240 في علاج أورام الجهاز الهضمي اللحمية |
| تطوير وتوسيع نطاق خط إنتاج الأدوية لدينا | تفاوضنا على ترخيص MTX240 من شركة أوتسوكا خلال النصف الثاني من عام 2025 ووقعنا اتفاقية الترخيص والتعاون في أوائل فبراير 2026 تم إصدار براءة الاختراع الأمريكية التي تغطي "تحضيرات واستخدام جسيمات الراباميسين النانوية عن طريق الفم" في فبراير | تعيين شركة تصنيع متعاقدة لتصنيع مستلزمات التجارب السريرية لدراسة المرحلة 1ب/2أ لعقار MTX240 في أورام الجهاز الهضمي اللحمية (GIST)، وبدء دراسة المرحلة 1ب/2أ لعقار MTX240 في أورام الجهاز الهضمي اللحمية (GIST). البدء بتجارب ما قبل السريرية لدعم مؤشرات إضافية محتملة، ويفضل أن تكون مؤشرات للأمراض النادرة، لاستخدام توليميدون البحث عن أصول إضافية في مرحلة ما قبل تقديم طلب دواء جديد (ما قبل IND) و/أو في المرحلة السريرية للاستحواذ عليها أو ترخيصها توسيع محفظة براءات الاختراع لدينا لتشمل الاختراعات الجديدة والفروع لتعزيز مجموعات براءات الاختراع الحالية |
| تأمين تمويل طويل الأجل، ويفضل أن يكون غير مخفف لحقوق الملكية للشركة | في شهر مايو، أعلنا أن شريكنا، إمتورا للعلوم الحيوية، قد حصل بنجاح على تمويل إضافي بقيمة 3.0 مليون دولار (ليصل الإجمالي إلى 20.0 مليون دولار) من معهد تكساس للوقاية من السرطان والبحوث ("CPRIT"). في ديسمبر، أعلنا عن تمويل بقيمة 10 ملايين دولار بسعر 3.28 دولار لكل سند إيداع أمريكي، مع إصدار ضمانين من الفئة L لكل سند إيداع أمريكي. | تأمين المرخص لهم و/أو شركاء التطوير المشترك لبرنامج eRapa في أوروبا واليابان البحث عن مصادر أخرى محتملة لرأس المال طويل الأجل لدعم برامج تطوير الشركة |
نموذج العمل
بعد أن نجحنا في توسيع نطاق منتجاتنا الداخلية، يتمثل نموذج أعمالنا في إضافة قيمة إلى برامج التطوير الخاصة بنا من خلال دفعها عبر التجارب السريرية قبل البحث عن شركاء لإكمال الدراسات في المراحل المتأخرة وتسويق المنتجات.
تطوير
نعتزم بناء محفظة متوازنة من الأصول قيد التطوير السريري، مع التركيز بشكل مثالي على مؤشرات الجهاز الهضمي والأورام. حصل دواء eRapa على ترخيص في أبريل 2024، ويخضع حاليًا لتجربة سريرية من المرحلة الثالثة لعلاج داء السلائل الورمي الغدي العائلي (FAP)، بالإضافة إلى دراسة جارية من المرحلة الثانية لعلاج سرطان المثانة غير الغازي للعضلات (NMIBC). حصل دواء MTX240 على ترخيص في فبراير 2026، وهو جاهز للمرحلة الأولى لعلاج أورام الجهاز الهضمي اللحمية (GIST). أما دواء Tolimidone، الذي حصل على ترخيص في ديسمبر 2023، فهو في المرحلة الثانية (أ) ويجري تطويره مبدئيًا لعلاج داء السكري من النوع الأول (T1D).
تصنيع
لا نعتزم إنشاء قدرات تصنيعية خاصة بنا. أما بالنسبة لمستلزمات التجارب السريرية، فنحن نستعين بمصنّعين متعاقدين حاصلين على شهادة ممارسات التصنيع الجيدة (GMP).
التسويق التجاري
بمجرد إثبات جدوى الفكرة، نعتزم ترخيص منتجاتنا لشريك يتولى إكمال التطوير السريري، ثم تسويقها وبيعها في المنطقة المرخصة. إضافةً إلى استرداد تكاليف التطوير، يُتوقع من الشريك دفعات مرحلية بناءً على أهداف المبيعات وحقوق الملكية. ولأن برنامج المرحلة الثالثة لعقار إيرابا في علاج داء السلائل الورمي الغدي العائلي ممول بشكل كبير بمنحة من مركز أبحاث السرطان في إلينوي (CPRIT) ومساهمة مماثلة من الشركة، فإن تسويق إيرابا في علاج هذا الداء من قبل الشركة يبقى خيارًا مطروحًا.
تتضمن خطة تطويرنا حاليًا أربعة مشاريع، جميعها في المرحلة السريرية، على النحو التالي:
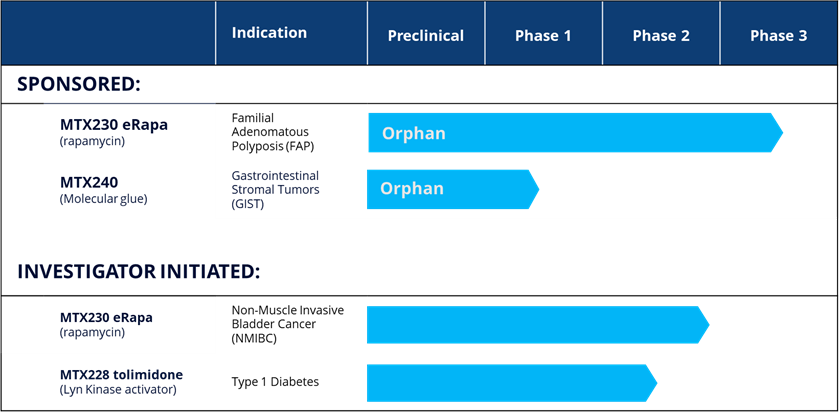
الأصول في المرحلة السريرية
إيرابا
إيرابا عبارة عن تركيبة كبسولات فموية مسجلة الملكية من الراباميسين، المعروف أيضًا باسم سيروليموس. الراباميسين هو مثبط لـ mTOR (الهدف الثديي للراباميسين). وقد ثبت أن لـ mTOR دورًا هامًا في مسار الإشارات الذي ينظم استقلاب الخلايا ونموها وتكاثرها، ويتم تنشيطه أثناء تكوين الأورام.>1 الراباميسين معتمد في الولايات المتحدة لعلاج رفض الأعضاء في عمليات زراعة الكلى تحت اسم راباميون® (شركة فايزر). من خلال استخدام تقنية النانو والبوليمرات الحساسة للأس الهيدروجيني، صُممت إيرابا لمعالجة انخفاض التوافر الحيوي، وتغير الحركية الدوائية، والسمية المرتبطة عمومًا بالأشكال المتوفرة حاليًا من الراباميسين.
داء السلائل الورمي الغدي العائلي (FAP)
يتميز داء السلائل العائلي (FAP) بتكاثر الزوائد اللحمية في القولون و/أو المستقيم، ويحدث عادةً في منتصف سنوات المراهقة. لا يوجد علاج معتمد لمرضى FAP، حيث تبقى المراقبة النشطة والاستئصال الجراحي للقولون و/أو المستقيم هما المعيار العلاجي. في حال عدم العلاج، يؤدي FAP عادةً إلى سرطان القولون و/أو المستقيم. يوجد عامل وراثي مهم في FAP، حيث تتراوح نسبة الإصابة به بين حالة واحدة لكل 5000 إلى 10000 شخص في الولايات المتحدة ، وحالة واحدة لكل 11300 إلى 37600 شخص في أوروبا. حصل دواء eRapa على تصنيف دواء اليتيم في الولايات المتحدة وأوروبا. ومن الجدير بالذكر أنه ثبت فرط تنشيط mTOR في زوائد FAP اللحمية، مما يؤكد جدوى استخدام مثبط mTOR قوي وآمن مثل eRapa لعلاج FAP. حصل eRapa على تصنيف المسار السريع من إدارة الغذاء والدواء الأمريكية في فبراير 2025.
عُرضت نتائج المرحلة الثانية من الدراسة في مؤتمرين علميين بارزين خلال الربع الثاني من عام 2024. وبعد اجتماع إيجابي من النوع (ج) مع إدارة الغذاء والدواء الأمريكية، تم وضع الصيغة النهائية لبروتوكول المرحلة الثالثة من التجارب السريرية. تُعرف هذه المرحلة باسم "سيرينتا"، وهي دراسة متعددة المراكز، مزدوجة التعمية، ومضبوطة بالغفل، تُجرى على مرضى معرضين لخطر الإصابة بداء السلائل الورمي الغدي العائلي (FAP). تخطط الدراسة لتجنيد 168 مريضًا يتم توزيعهم عشوائيًا بنسبة 2:1 (دواء:غفل) في 30 موقعًا أو أكثر في الولايات المتحدة وأوروبا، مع اعتبار الوقت اللازم للوصول إلى حدث محدد للبقاء على قيد الحياة دون تطور المرض نقطة النهاية الأولية. كما سيتم قياس جودة الحياة. من المتوقع أن تستغرق الدراسة 18 شهرًا، وهي مدعومة بمنحة غير مخففة بقيمة 20 مليون دولار أمريكي من مركز أبحاث الوقاية من السرطان في إلينوي (CPRIT).
سرطان المثانة غير الغازي للعضلات (NMIBC)
يشير سرطان المثانة غير الغازي للعضلات (NMIBC) إلى الأورام التي تُكتشف في النسيج المُبطّن للسطح الداخلي للمثانة. العلاج الأكثر شيوعًا هو استئصال ورم المثانة عبر الإحليل، يليه حقن لقاح باسيل كالميت غيران (BCG) داخل المثانة، مع العلاج الكيميائي بناءً على تقييم خطر عودة الورم. يُعدّ سرطان المثانة غير الغازي للعضلات رابع أكثر أنواع السرطان شيوعًا بين الرجال، حيث تبلغ نسبة الإصابة به 10.1 لكل 100,000 رجل و2.5 لكل 100,000 امرأة . وقد اكتمل تسجيل 166 مريضًا في تجربة سريرية جارية من المرحلة الثانية، مزدوجة التعمية، ومضبوطة بالغفل، لعلاج سرطان المثانة غير الغازي للعضلات، وتتمثل نقاط النهاية الأولية في السلامة/التحمل والبقاء على قيد الحياة دون انتكاس بعد 12 شهرًا من العلاج. وتحظى دراسة المرحلة الثانية بدعم منحة غير مخففة بقيمة 2.8 مليون دولار أمريكي من المعهد الوطني للسرطان، التابع للمعاهد الوطنية للصحة.
MTX240
MTX240، الذي اكتشفه أوتسوكا وكان يُعرف سابقًا بالرمز OPB-171775، هو مادة لاصقة جزيئية مبتكرة نعتزم تطويرها مبدئيًا لعلاج أورام الجهاز الهضمي اللحمية (GIST). تعمل هذه المادة اللاصقة الجزيئية لـ MTX240 على ربط بروتينين داخل خلويين، هما PDE3A وSLFN12، واللذان تُعبر عنهما خلايا سرطان GIST بشكل مشترك، لتكوين مركب مستقر. يُثبّت هذا التفاعل بروتين SLFN12، مما يُمكّنه من تحفيز موت الخلايا المبرمج بوساطة RNase في خلايا GIST من خلال آلية مستقلة عن إشارات KIT أو PDGFR. ينجم سرطان GIST في الغالب عن طفرات مُنشّطة في مستقبلات التيروزين كيناز KIT أو PDGFR. على الرغم من أن مثبطات التيروزين كيناز (TKIs) مثل إيماتينيب وسونيتينيب وريجورافينيب قد حسّنت بشكل ملحوظ نتائج علاج مرضى GIST، إلا أن المقاومة تتطور دائمًا تقريبًا من خلال طفرات ثانوية في KIT أو PDGFR أو تنشيط مسارات إشارات بديلة. يمثل هذا تحديًا سريريًا كبيرًا مع خيارات علاجية محدودة للمرضى بعد استنفادهم جميع مثبطات التيروزين كيناز المتاحة. تُقدم تقنية اللصق الجزيئي نهجًا مبتكرًا يحفز تفاعلات بروتينية مُستهدفة، مما يوفر آلية عمل مميزة لمثبطات التيروزين كيناز التقليدية لعلاج أورام الجهاز الهضمي اللحمية (GIST)، وذلك عن طريق تحفيز موت الخلايا عبر مسار بديل لكيناز البروتين المنشط بالمايتوجين (MAPKinase). صُمم MTX240 للتغلب على آليات المقاومة التي تجعل أورام الجهاز الهضمي اللحمية المقاومة لمثبطات التيروزين كيناز غير مستجيبة لها.
أورام اللحمة المعدية المعوية (GIST)
يُعدّ ورم الجهاز الهضمي اللحمي (GIST) ورمًا خبيثًا نادرًا في الجهاز الهضمي، حيث يُشخّص حوالي 6000 مريض سنويًا في الولايات المتحدة الأمريكية، وهناك حاجة طبية ملحة غير مُلبّاة للمرضى الذين يُصابون بمقاومة لمثبطات التيروزين كيناز (TKI). يُعاني ما يقرب من 10-15% من مرضى GIST من مقاومة أولية، أو يُصابون بمقاومة ثانوية لمثبطات التيروزين كيناز المتاحة، مما يجعل خيارات العلاج لهؤلاء المرضى محدودة.
تبلغ قيمة سوق أورام الجهاز الهضمي اللحمية العالمية حوالي 1.3 مليار دولار ومن المتوقع أن تنمو بنسبة 6-10٪ سنويًا حتى عام 2032، مدفوعة بارتفاع معدل الإصابة وظهور خيارات علاجية جديدة تستهدف الأمراض المقاومة للعلاج.
يستوفي دواء GIST شروط الحصول على تصنيف دواء اليتيم في الولايات القضائية التنظيمية الرئيسية، مما يوفر مزايا تنظيمية محتملة وحوافز لدعم تطوير الأدوية.
توليميدون
اكتُشف دواء توليميدون في الأصل من قِبل شركة فايزر، وطُوّر خلال المرحلة الثانية من التجارب السريرية لعلاج قرحة المعدة. وقد أجرت فايزر برنامجًا واسع النطاق قبل التجارب السريرية لتحديد خصائص توليميدون الدوائية، وحركيته الدوائية، واستقلابه، وسميته. إلا أن فايزر أوقفت تطوير الدواء لعدم فعاليته لهذا الغرض في المرحلة الثانية (أ). يُعد توليميدون مُنشطًا انتقائيًا لإنزيم لين كيناز، الذي يزيد من فسفرة ركيزة الأنسولين-1، وبالتالي يُضخّم سلسلة الإشارات التي تبدأ بارتباط الأنسولين بمستقبله.
داء السكري من النوع الأول (T1D)
في داء السكري من النوع الأول، يهاجم جهاز المناعة في الجسم خلايا بيتا في البنكرياس، مما يؤدي إلى عجزها عن إنتاج الأنسولين اللازم لتنظيم مستوى الجلوكوز في الدم. لا تزال أسباب داء السكري من النوع الأول غير مفهومة تمامًا، ولا يوجد علاج شافٍ له حاليًا. ويعتمد مرضى داء السكري من النوع الأول على تناول الأنسولين يوميًا (عن طريق الحقن أو التسريب الوريدي).
نعمل على تطوير دواء توليميدون لعلاج داء السكري من النوع الأول. وباعتباره مُنشطًا لكيناز لين، فقد أظهرت التجارب ما قبل السريرية أن توليميدون يلعب دورًا في بقاء خلايا بيتا وتكاثرها. وإذا ما تأكدت هذه النتائج في الدراسات السريرية، فقد يكون لتوليميدون القدرة على تعديل مسار المرض وتغيير نموذج علاج داء السكري من النوع الأول. يُصيب داء السكري من النوع الأول حوالي 8.4 مليون شخص حول العالم، ويتم تشخيص حوالي 500,000 حالة جديدة سنويًا .
مراجعة الرئيس التنفيذي
مقدمة
في عام 2025، انصبّ تركيزنا الأساسي على بدء المرحلة الثالثة من التجارب السريرية لعقار سيرينتا (Serenta) لعلاج داء السلائل الورمي الغدي العائلي (FAP). كما بُذلت جهود كبيرة في إجراءات التدقيق والتفاوض بشأن اتفاقية الترخيص والتعاون الخاصة بعقار MTX240، والتي وُقّعت في أوائل فبراير 2026.
تحديثات البحث والتطوير
إيرابا
حصلنا على ترخيص eRapa، وهو تركيبة خاصة من الراباميسين، من شركة Rapamycin Holdings, Inc. d/b/a Emtora Biosciences, Inc. ("Emtora") في أبريل 2024. وقد أحرزنا تقدمًا كبيرًا في برنامج المرحلة 3 الخاص بنا لـ eRapa في FAP خلال عام 2025 وحققنا عددًا من المعالم المهمة كما هو موضح أدناه.
في مارس 2025، أعلنا عن تعيين شركة Precision for Medicine, LLC ("Precision") كجهة بحثية تعاقدية لإدارة الجزء الأوروبي من المرحلة الثالثة من تجاربنا السريرية. تتمتع Precision بخبرة تزيد عن 20 عامًا، وتستند سمعتها إلى كوادرها عالية الكفاءة والمتخصصة علاجيًا، وعلمائها وأطبائها ذوي الخبرة، ومختبراتها المتخصصة المتطورة، وقدراتها المتميزة في حل المشكلات. أجرت Precision 333 تجربة سريرية في مجال الأمراض النادرة، ويعمل لديها أكثر من 700 عضو فريق في أوروبا موزعين على 11 موقعًا.
كذلك، في مارس 2025، أفدنا بأننا عقدنا اجتماعًا مثمرًا من النوع (ج) مع إدارة الغذاء والدواء الأمريكية، تضمن مناقشة الخطة الإحصائية، وقاعدة بيانات السلامة، والأهم من ذلك، نقطة نهاية مركبة لتجربة سيرينتا من المرحلة الثالثة. وقدّم ممثلو إدارة الغذاء والدواء من قسمي أمراض الجهاز الهضمي والأورام مساهمات قيّمة في البرنامج المقترح، مما وفّر مسارًا واضحًا للمضي قدمًا في وضع الصيغة النهائية للبروتوكول.
بعد بدء أول موقع سريري في الولايات المتحدة في يونيو 2025، تم تسجيل أول مريض أمريكي في أغسطس 2025. وفي نوفمبر 2025، حصلنا على موافقة من وكالة الأدوية الأوروبية (EMA) على طلبنا لإجراء تجربة سريرية للمرحلة الثالثة، وتم تسجيل أول مريض أوروبي في ديسمبر 2025. وحتى 16 مارس، كان هناك 22 موقعًا سريريًا نشطًا و37 مريضًا مسجلين في دراسة سيرينتا.
وشملت الإنجازات الأخرى التي تحققت في عام 2025 الحصول على تصنيف المسار السريع من إدارة الغذاء والدواء الأمريكية وتصنيف الدواء اليتيم من وكالة الأدوية الأوروبية.
من المتوقع أن تستغرق دراسة المرحلة الثالثة حوالي 18 شهرًا لتجنيد جميع المرضى البالغ عددهم 168 مريضًا، وسيتم إغلاق قاعدة البيانات بعد 75 حدثًا، وهو ما يُتوقع أن يكون في النصف الثاني من عام 2029.
وقد تم تسجيل جميع المرضى الـ 166 في المرحلة الثانية من العلاج المناعي لـ eRapa في سرطان المثانة غير الغازي للعضلات، وهي دراسة جارية مزدوجة التعمية ومضبوطة بالغفل، ومن المتوقع أن يتم الإعلان عن نتائجها في الربع الثالث من عام 2026.
MTX240
في فبراير 2026، أعلنا عن توقيع اتفاقية ترخيص وتعاون مع شركة أوتسوكا لتطوير وتسويق جهاز MTX240. وبموجب بنود هذه الاتفاقية، نتمتع بحقوق حصرية لتطوير وتسويق الجهاز عالميًا باستثناء اليابان، حيث تحتفظ أوتسوكا بحقوقها. تضمنت الاتفاقية رسومًا أولية رمزية، وتنص على دفع رسوم إضافية عند تحقيق مرحلة تطويرية واحدة، بالإضافة إلى رسوم موافقة تتراوح بين 10% و20%. علاوة على ذلك، تُدفع عوائد متدرجة تتراوح بين 5% و5% على صافي مبيعات جهاز MTX240.
يتميز MTX240، باعتباره مادة لاصقة جزيئية، بآلية عمل فريدة مقارنةً بمثبطات التيروزين كيناز، وهي العلاج القياسي الحالي لأورام الجهاز الهضمي اللحمية (GIST)، والتي قد تفقد جميعها فعاليتها مع مرور الوقت نتيجة استمرار الطفرات. قد توفر آلية عمل MTX240 الجديدة فائدة سريرية لنسبة كبيرة من مرضى GIST، وليس فقط أولئك الذين طوروا مقاومة لمثبطات التيروزين كيناز. في نماذج زرع الأورام المشتقة من المرضى (PDX)، أظهر MTX240 فعالية مضادة للأورام تعتمد على الجرعة في النماذج المقاومة للإيماتينيب والسونيتينيب، بغض النظر عن حالة طفرة KIT.
يستفيد MTX240 من براءات اختراع تركيب المادة في الولايات المتحدة وأوروبا واليابان والعديد من البلدان الأخرى التي تمتد حتى عام 2037 باستثناء أي تمديد لفترة براءة الاختراع.
تتمثل خطوتنا الأولى في تصنيع كميات كافية من دواء MTX240 لإجراء التجارب السريرية، ثم البدء بدراسة مفتوحة التسمية من المرحلة 1ب/2أ بحلول نهاية العام. من المتوقع أن تتألف الدراسة من جزأين: جزء لتحديد الجرعة القصوى التي يتحملها المريض، يليه جزء موسع. من المرجح أن يشمل الجزء الموسع مرضى مصابين بأورام الجهاز الهضمي المقاومة لمثبطات التيروزين كيناز. من خلال التركيز على هذه الفئة من المرضى ذوي الاحتياجات العالية، نهدف إلى التحقق سريعًا من قدرة MTX240 على علاج المرضى الذين لا يستجيبون، أو لم يعودوا يستجيبون، للعلاج القياسي الحالي.
توليميدون
في ديسمبر 2023، حصلنا على الحقوق العالمية لتطوير وتسويق توليميدون. يدعم هذا المنتج بيانات ما قبل السريرية واسعة النطاق، وقد خضع للعلاج على أكثر من 700 مريض، وأظهر نتائج واعدة تدعم اختيارنا لعلاج داء السكري من النوع الأول. كخطوة أولى في التطوير السريري المستمر المخطط له لتوليميدون، بدأنا المرحلة الثانية (أ) من دراسة تأكيد الجرعة في معهد السكري بجامعة ألبرتا، حيث تم تسجيل أول مريض في يونيو 2025. تُجرى دراسة المرحلة الثانية (أ) بطريقة مفتوحة، ومن المتوقع أن تشمل حوالي 15 مريضًا مصابًا بداء السكري من النوع الأول، والذين سيتلقون علاج توليميدون لمدة ثلاثة أشهر، مع التركيز على قياس التغيرات في مستويات الببتيد C، ومستوى الهيموجلوبين السكري (HbA1c)، وعدد نوبات ارتفاع السكر في الدم.
MTX110
بسبب القيود المفروضة على الموارد، لم يتم تمويل برامج MTX110 لعلاج سرطان الدماغ النادر/اليتيم في عام 2025، وبالتالي تم استبعادها من خطة التطوير لدينا.
التمويل
سند إذني
في ديسمبر 2024، أصدرنا سندًا إذنيًا غير مضمون لشركة C/M Capital Master Fund LP بقيمة أصلية قدرها 600,000 دولار أمريكي، مع خصم إصدار أولي بنسبة 10%. كان السند التزامًا غير مضمون بفائدة سنوية قدرها 5%، وتم سداده بالكامل في ديسمبر 2025.
خط ائتمان الأسهم (ELOC)
في يناير 2025، أبرمنا اتفاقية قرض تقاعدي لمدة ثلاث سنوات بقيمة 35.0 مليون دولار مع صندوق C/M Capital Master Fund, LP. وخلال عام 2025، استخدمنا هذا القرض لجمع ما يقرب من 8.9 مليون دولار كعائدات إجمالية.
منحة CPRIT
في مايو 2025، أعلنا أن مركز أبحاث الوقاية من السرطان في إلينوي (CPRIT) قد منح منحة إضافية قدرها 3 ملايين دولار، ليصل إجمالي المنحة إلى 20 مليون دولار، لدعم المرحلة الثالثة من برنامج eRapa في علاج إدمان الكحول. ويشترط استلام هذه الأموال مساهمة مماثلة من الشركة.
عرض مسجل
في ديسمبر 2025، أغلقنا طرحًا مسجلاً لشهادات الإيداع الأمريكية (ADS) وسندات الضمان الممولة مسبقًا بسعر 3.28 دولارًا أمريكيًا للشهادة الواحدة، لجمع عائدات إجمالية قدرها 10 ملايين دولار أمريكي. كما أصدرنا 6.1 مليون سند ضمان من الفئة L قابلة للتنفيذ بسعر 3.28 دولارًا أمريكيًا على مدى خمس سنوات.
ترد تفاصيل إضافية عن التمويلات في "المراجعة المالية".
أوتلوك
سيكون تركيزنا الأساسي لعام 2026 ذا شقين: أولاً، مواصلة تسريع تسجيل المرضى في المرحلة الثالثة من تجربة Serenta التسجيلية في الولايات المتحدة وأوروبا، وذلك بإضافة بلدان ومواقع إضافية، وثانياً، تصنيع الإمدادات السريرية وبدء دراسة المرحلة 1ب/2أ لـ MTX240 في GIST.
كما كان الحال في السنوات القليلة الماضية، لا يزال تمويل شركات التكنولوجيا الحيوية الصغيرة والمتناهية الصغر يمثل تحديًا. يُمدد طرح الأسهم المسجل بقيمة 10 ملايين دولار في ديسمبر 2025 فترة استمرارنا حتى الربع الثالث من عام 2026، بينما يوفر خط ائتمان ELOC بقيمة 35 مليون دولار الذي وضعناه في فبراير 2025 مصدرًا احتياطيًا محتملاً لرأس المال.
1- تيان وآخرون، إشارات mTOR في السرطان ومثبطات mTOR في العلاج الموجه للأورام الصلبة، المجلة الدولية للعلوم الجزيئية. فبراير 2019؛ 20(3): 755
2 www.rarediseases.org
3. www.orpha.net
- كاسيل وآخرون، مجلة علم الأورام العالمية. يونيو 2019؛ 10(3): 123-131
5- تشو، هـ.، وآخرون (2023). تحديث علم الأوبئة، ومعدلات البقاء على قيد الحياة، والعلاج الأولي في أورام اللحمة المعدية المعوية: تحليل قائم على السكان. بي إم جيه أوبن، 13(7)، e072945. https://doi.org/10.1136/bmjopen-2023-072945
6. داتا بريدج لأبحاث السوق. (2023). حجم سوق أورام اللحمة المعدية المعوية، والاتجاهات، والتوقعات (2024-2032). تم استرجاعه من https://www.databridgemarketresearch.com/reports/global-gastrointestinal-stromal-tumor-market
7 Medicina أبريل 2023
مراجعة مالية
مقدمة
تأسست شركة Biodexa Pharmaceuticals PLC كشركة في 12 سبتمبر 2014 ومقرها في إنجلترا وويلز.
التحليل المالي
مؤشرات الأداء الرئيسية
| 2025 | 2024 | يتغير | |
| نفقات البحث والتطوير | 3.96 مليون جنيه إسترليني | 5.44 مليون جنيه إسترليني | (27.2)٪ |
| البحث والتطوير كنسبة مئوية من تكاليف التشغيل | 45% | 59% | غير متوفر |
| صافي التدفق النقدي الداخل/الخارج للسنة | 6.87 مليون جنيه إسترليني | (4.30 مليون جنيه إسترليني) | غير محدد |
| ============ | ============ | ============ | |
ربح
بلغت الإيرادات خلال الفترتين صفر جنيه إسترليني. واختتمت آخر شراكات الشركة في مجال البحث والتطوير في سبتمبر 2023.
نفقات البحث والتطوير
كانت تكاليف البحث والتطوير التي تم تحليلها حسب مؤشر مشروع التطوير كما يلي:
| السنة المنتهية في 31 ديسمبر | 2025 | 2024 | |
| ألف جنيه إسترليني | ألف جنيه إسترليني | ||
| MTX230 eRapa | |||
| داء السلائل الورمي الغدي العائلي (بعد خصم المنحة) | 1338 | 1627 | |
| سرطان المثانة غير الغازي للعضلات | 154 | 284 | |
| إجمالي أوروبا | 1492 | 1911 | |
| توليميدون MTX228 | |||
| داء السكري من النوع الأول | 383 | 1093 | |
| إجمالي توليميدون | 383 | 1093 | |
| MTX110 (بانوبينوستات) | |||
| ورم دبقي منتشر في الخط المتوسط | - | (6) | |
| ورم أرومي دبقي متكرر | 36 | 635 | |
| ورم أرومي نخاعي | - | - | |
| إجمالي MTX110 (بانوبينوستات) | 36 | 629 | |
| دراسات ما قبل السريرية الأخرى | - | 102 | |
| تكاليف البحث والتطوير | 2050 | 1702 | |
| البحث والتطوير الشامل | 3961 | 5437 | |
تظهر تكاليف دواء MTX230 eRapa لعلاج داء السلائل الورمي الغدي العائلي أعلاه بعد خصم دخل المنحة. ويتم تحليل ذلك على النحو التالي:
| السنة المنتهية في 31 ديسمبر | 2025 | 2024 | |
| ألف جنيه إسترليني | ألف جنيه إسترليني | ||
| دخل المنح | (4458) | (1215) | |
| التكاليف الإجمالية | 5796 | 2842 | |
| صافي المصروفات في بيان الدخل | 1338 | 1627 | |
| نسبة التكاليف المخصصة من منحة CPRIT | 77% | 43% | |
بلغت تكاليف البحث والتطوير 3.96 مليون جنيه إسترليني، بانخفاض قدره 1.48 مليون جنيه إسترليني، أو 27% مقارنةً بعام 2024 (5.44 مليون جنيه إسترليني في عام 2024). وانخفضت نسبة تكاليف البحث والتطوير من إجمالي تكاليف التشغيل إلى 45% من 59% في العام السابق. ويعكس هذا الانخفاض في تكاليف البحث والتطوير في عام 2025 بشكل رئيسي انخفاضًا في الإنفاق قدره 0.71 مليون جنيه إسترليني على الدراسات ما قبل السريرية وتكاليف تصنيع MTX228، و0.60 مليون جنيه إسترليني على دراسة MTX110 MAGIC-G1 لعلاج الورم الأرومي الدبقي المتكرر، و0.44 مليون جنيه إسترليني على MTX230 eRapa (بعد خصم دخل منحة CPRIT). وبلغت نسبة تكاليف MTX230 (eRapa) التي أمكن تعويضها من تمويل المنحة خلال هذه الفترة 77% مقارنةً بـ 43% في عام 2024. ونتوقع أن تصل هذه النسبة إلى 67% على مدار فترة المنحة.
التكاليف الإدارية
ارتفعت التكاليف الإدارية خلال العام بمقدار 1.04 مليون جنيه إسترليني لتصل إلى 4.84 مليون جنيه إسترليني (مقابل 3.79 مليون جنيه إسترليني في عام 2024)، أي بزيادة قدرها 27%. ويعود سبب هذه الزيادة إلى تقلبات أسعار الصرف الأجنبي بقيمة 0.44 مليون جنيه إسترليني، وزيادة في أتعاب الخدمات المهنية بقيمة 0.73 مليون جنيه إسترليني، قابلها انخفاض في المدفوعات القائمة على الأسهم بقيمة 0.10 مليون جنيه إسترليني.
في عام 2025، خصصت الشركة 1.72 مليون جنيه إسترليني كمصروفات على الرسوم القانونية والمهنية المتعلقة بصفقة التمويل الناجحة في ديسمبر، والاستحواذ على ترخيص أوتسوكا الذي اكتمل في عام 2026 وعمليات الاستحواذ الملغاة، و0.37 مليون جنيه إسترليني كرسوم التزام مقدمة غير نقدية لخط ائتمان ELOC، وهذا بالمقارنة مع 0.88 مليون جنيه إسترليني تم إنفاقها في عام 2024 على معاملات مماثلة.
تكاليف الموظفين
خلال العام، انخفض متوسط عدد الموظفين إلى 11 موظفًا (2024: 13 موظفًا). وارتفعت التكلفة الإجمالية للموظفين بنسبة 1% لتصل إلى 2.17 مليون جنيه إسترليني (2024: 2.15 مليون جنيه إسترليني)، مدفوعةً بزيادة في الأجور والرواتب قدرها 0.14 مليون جنيه إسترليني.
الإيرادات والمصروفات المالية
تضمنت إيرادات التمويل في عامي 2025 و2024 مكاسب من التزامات مالية مشتقة تم تسويتها عن طريق حقوق الملكية بقيمة 2.30 مليون جنيه إسترليني (2024: 3.22 مليون جنيه إسترليني). وقد نتجت هذه المكاسب عن انخفاض سعر سهم شركة بيوديكسا. بالإضافة إلى ذلك، حققت الشركة فوائد على الودائع النقدية.
مصروفات التمويل في عامي 2024 و2025 المتعلقة بالتزامات الإيجار، والفائدة المخصومة على المقابل المؤجل، والفائدة على سند إذني صادر في ديسمبر 2024.
الضرائب
خلال عامي 2025 و2024، قمنا بتسجيل إعفاءات ضريبية للبحث والتطوير في المملكة المتحدة بقيمة 0.11 مليون جنيه إسترليني و0.25 مليون جنيه إسترليني فيما يتعلق بنفقات البحث والتطوير المتكبدة.
الإنفاق الرأسمالي
بلغت قيمة مشتريات الأصول الثابتة الملموسة في عام 2025 مبلغ 2000 جنيه إسترليني (مقابل 0.01 مليون جنيه إسترليني في عام 2024)، وتعلقت هذه المشتريات بشراء معدات تقنية المعلومات. وخلال العام نفسه، اتخذت الشركة قرارًا بإغلاق مختبرها في كارديف والتخلص من معظم معداته. ويتماشى هذا مع استراتيجية الشركة المذكورة أعلاه.
التدفق النقدي
بلغ صافي التدفق النقدي الخارج من الأنشطة التشغيلية في عام 2025 مبلغ 5.59 مليون جنيه إسترليني (2024: تدفق خارج قدره 12.26 مليون جنيه إسترليني) مدفوعًا بخسارة صافية قدرها 6.38 مليون جنيه إسترليني (2024: خسارة قدرها 5.73 مليون جنيه إسترليني) وبعد تحركات إيجابية في رأس المال العامل قدرها 1.72 مليون جنيه إسترليني (2024: سالب 3.74 مليون جنيه إسترليني)، وضرائب محصلة قدرها 0.71 مليون جنيه إسترليني (2024: 0.13 مليون جنيه إسترليني)، وتعديلات سلبية صافية أخرى لبنود غير نقدية بلغ مجموعها 1.63 مليون جنيه إسترليني (2024: سالب 2.93 مليون جنيه إسترليني).
بلغ صافي التدفقات النقدية الخارجة من أنشطة الاستثمار في عام 2025 مبلغ 0.58 مليون جنيه إسترليني (مقابل 0.60 مليون جنيه إسترليني في عام 2024)، وشمل ذلك شراء عقارات ومنشآت ومعدات بقيمة 2000 جنيه إسترليني (مقابل 0.01 مليون جنيه إسترليني في عام 2024)، ودفع أقساط مؤجلة لرخصة eRapa بقيمة 0.69 مليون جنيه إسترليني (مقابل 0.77 مليون جنيه إسترليني في عام 2024). وقد تم تعويض هذه التدفقات النقدية الخارجة بدخل فوائد من الودائع المصرفية بقيمة 0.09 مليون جنيه إسترليني (مقابل 0.18 مليون جنيه إسترليني في عام 2024).
وقد نتج عن تدفق أنشطة التمويل في عام 2025 مبلغ 13.04 مليون جنيه إسترليني (2024: تدفق 8.56 مليون جنيه إسترليني) من عائدات إصدارات الأسهم البالغة 13.75 مليون جنيه إسترليني (2024: 8.31 مليون جنيه إسترليني) من استخدام اتفاقية ELOC، وعائدات حافز الضمان في مايو 2025 وعائدات الطرح المسجل في ديسمبر 2025. ويتم تعويض ذلك بسداد القروض (بما في ذلك الفائدة) بقيمة 0.46 مليون جنيه إسترليني ومدفوعات التزامات الإيجار بقيمة 0.25 مليون جنيه إسترليني (2024: 0.19 مليون جنيه إسترليني).
ونتيجة لما سبق، بلغ صافي التدفق النقدي الداخل لهذا العام 6.87 مليون جنيه إسترليني (2024: تدفق نقدي خارج قدره 4.30 مليون جنيه إسترليني).
التغير في نسبة الإيداعات الأمريكية والقيمة الاسمية للأسهم العادية
في 31 يوليو 2025، أجرت الشركة تغييرًا في نسبة أسهمها العادية من كل إيصال إيداع أمريكي يمثل 10000 سهم عادي إلى كل إيصال إيداع أمريكي يمثل 100000 سهم عادي.
في اجتماع الجمعية العمومية المنعقد بتاريخ 11 يونيو 2025، وافق المساهمون على تقسيم وإعادة تصنيف أسهم الشركة العادية المصدرة، بقيمة 0.00005 جنيه إسترليني للسهم الواحد، إلى سهم عادي واحد بقيمة 0.000001 جنيه إسترليني و49 سهمًا مؤجلًا من الفئة "د" بقيمة 0.000001 جنيه إسترليني للسهم الواحد. تتمتع الأسهم المؤجلة من الفئة "د" بحقوق محدودة، وهي عمليًا عديمة القيمة.
في 18 مارس 2026، أعلنت الشركة عن تغيير في نسبة أسهمها العادية من كل إيصال إيداع أمريكي يمثل 100,000 سهم عادي إلى كل إيصال إيداع أمريكي يمثل 500,000 سهم عادي.
التمويل
خط ائتمان الأسهم ("ELOC")
في يناير 2025، أبرمنا اتفاقية شراء أوراق مالية، أو ما يُعرف بخط ائتمان الأسهم ("ELOC")، مع شركة C/M المُنشأة حديثًا. وبموجب شروط هذا الخط، يحق لنا، لا أن نكون مُلزمين، ببيع ما يصل إلى 35 مليون دولار أمريكي من شهادات الإيداع الأمريكية (ADS) المُصدرة حديثًا إلى شركة C/M على مدى 36 شهرًا، ما لم يتم إنهاء خط الائتمان. وكمقابل لتنفيذ وتسليم خط الائتمان، وافقنا على دفع رسوم التزام ("رسوم الالتزام") قدرها 875,000 دولار أمريكي نقدًا، منها (أ) 612,500 دولار أمريكي تُدفع لشركة C/M عند توقيع خط الائتمان، و(ب) يُدفع المبلغ المتبقي بالتناسب مع تسليم أي شهادات إيداع أمريكية تم بيعها بموجب خط الائتمان. وكان لنا الحق في إصدار شهادات إيداع أمريكية تُمثل قيمة الجزء المُطبق من رسوم الالتزام. لقد دفعنا رسوم الالتزام الأولية البالغة 612,500 دولارًا أمريكيًا من خلال إصدار 140,080 سهمًا إيداعيًا للمشتري.
يجوز لنا توجيه شركة C/M لشراء عدد محدد من أسهم الإيداع الأمريكية (ADS) لا يتجاوز 2.5 مليون دولار أمريكي في أي يوم، بسعر يُحدد بناءً على صيغة رياضية، وعادةً ما يكون 95% من سعر الإغلاق في اليوم السابق. وحتى 31 ديسمبر 2025، جمعت الشركة عائدات إجمالية قدرها 8.92 مليون دولار أمريكي من خطاب تسهيلات رأس المال المساهم (ELOC).
استدراج للحصول على مذكرة توقيف
في مايو 2025، أبرمنا اتفاقيات خطية مع بعض حاملي سندات الشراء القائمة من الفئات E وH وJ وK لتخفيض سعر ممارسة هذه السندات إلى 0.31 دولار أمريكي للسهم الواحد. مارس حاملو هذه السندات ما مجموعه 200,433 سند شراء، وهو ما يمثل العدد نفسه من شهادات الإيداع الأمريكية. وقد حصلنا على عائدات إجمالية تقارب 62,000 دولار أمريكي، قبل خصم مصاريف الطرح. لم تصدر الشركة سندات شراء جديدة لتحل محل السندات التي تم ممارستها، ولم تستعن بوكيل طرح لتسهيل هذه العملية.
عرض مسجل
في ديسمبر 2025، أتممنا طرحًا مسجلاً للمستثمرين المؤسسيين لبيع (أ) ما مجموعه 157,000 شهادة إيداع أمريكية، و(ب) ما مجموعه 2,891,781 أمر شراء ممول مسبقًا قابل للتنفيذ لأسهم إيداع بسعر 3.28 دولار أمريكي للسهم الواحد، وسعر 3.2799 دولار أمريكي لأمر الشراء الممول مسبقًا. وكانت أوامر الشراء الممولة مسبقًا قابلة للتنفيذ فورًا. إضافةً إلى ذلك، أصدرنا وبعنا للمستثمرين أوامر شراء من الفئة L لـ 6,097,562 سهم إيداع بسعر 3.28 دولار أمريكي للسهم الواحد. أوامر الشراء من الفئة L قابلة للتنفيذ فورًا وتنتهي صلاحيتها بعد خمس سنوات من تاريخ الإصدار. وقد بلغ إجمالي العائدات 10 ملايين دولار أمريكي قبل خصم رسوم وكيل التوزيع ومصاريف الطرح ذات الصلة.
سند إذني
تم سداد السند الإذني الصادر في ديسمبر 2024 بقيمة 600,000 دولار بالكامل خلال العام.
منحة CPRIT
في مايو 2025، أعلنا أن شريكنا في التعاون، إمتورا، قد حصل على منحة إضافية قدرها 3 ملايين دولار من مركز أبحاث الوقاية من السرطان في إيطاليا (CPRIT). وبذلك، ارتفع إجمالي المنح التي قدمها المركز لدعم برنامج المرحلة الثالثة لتسجيل عقار إيرابا لعلاج داء السلائل الورمي الغدي العائلي (FAP) إلى 20 مليون دولار. ويشترط للحصول على مبلغ الـ 3 ملايين دولار أن تقدم الشركة مبلغًا مماثلًا قدره 3 ملايين دولار.
استمرارية العمل - عدم اليقين المادي
تكبدت المجموعة والشركة خسائر صافية وتدفقات نقدية خارجة كبيرة من النقد المستخدم في الأنشطة التشغيلية خلال السنوات الماضية في إطار تطوير محفظتها الاستثمارية. وفي السنة المنتهية في 31 ديسمبر 2025، تكبدت المجموعة خسارة موحدة قدرها 6.38 مليون جنيه إسترليني وتدفقات نقدية سلبية من العمليات التشغيلية قدرها 5.59 مليون جنيه إسترليني. وفي 31 ديسمبر 2025، بلغ العجز المتراكم للمجموعة 155.81 مليون جنيه إسترليني.
يعتمد استمرار المجموعة في المستقبل على قدرتها على جمع السيولة من خلال أنشطة التمويل لتمويل خططها التنموية إلى حين تحقيق مراحل محددة و/أو الحصول على عوائد من شراكاتها في أصول الشركة. وقد يؤدي عجز المجموعة عن جمع رأس المال عند الحاجة إلى تأثير سلبي على وضعها المالي وقدرتها على تنفيذ استراتيجياتها التجارية.
يرى مجلس الإدارة أن هناك خيارات كافية ووقتًا مناسبًا لتأمين تمويل إضافي للشركة، وبعد دراسة أوجه عدم اليقين، يرى المجلس أنه من المناسب الاستمرار في اعتماد مبدأ استمرارية النشاط في إعداد هذه البيانات المالية. ولذلك، عُرضت البيانات المالية الموحدة للمجموعة على أساس استمرارية النشاط، الذي يأخذ في الاعتبار تحقيق الأصول وسداد الالتزامات في سياق العمل المعتاد.
في 31 ديسمبر 2025، بلغ رصيد المجموعة من النقد وما يعادله 8.53 مليون جنيه إسترليني. وقد أعدّ مجلس الإدارة توقعات التدفقات النقدية، ودرس احتياجات المجموعة من التدفقات النقدية للسنوات الثلاث المقبلة، بما في ذلك فترة الاثني عشر شهرًا من تاريخ اعتماد البيانات المالية الموحدة. وتشير هذه التوقعات إلى الحاجة إلى تمويل إضافي في الربع الثالث من عام 2026، بافتراض، من بين أمور أخرى ، استمرار بعض برامج التطوير والأنشطة التشغيلية الأخرى وفقًا للخطة الحالية. وبموجب خط ائتمان حقوق الملكية البالغ 35 مليون دولار أمريكي، كما هو موضح أعلاه، يجوز للشركة توجيه شركة C/M لشراء أسهم الإيداع الأمريكية (مع مراعاة بعض القيود) واستلام العائدات وفقًا لسعر محدد. ولا يوجد ما يضمن قدرة الشركة على استخدام خط ائتمان حقوق الملكية أو الحصول على تمويل من مصادر أخرى بالقدر اللازم لتمويل عملياتها. وفي 31 ديسمبر 2025، لا يزال مبلغ 26.08 مليون دولار أمريكي غير مسحوب من خط ائتمان حقوق الملكية.
يرى مجلس الإدارة أن بيئة تمويل شركات التكنولوجيا الحيوية الصغيرة والمتناهية الصغر لا تزال مليئة بالتحديات. ورغم أن هذا قد يتيح فرصًا للاستحواذ أو الاندماج مع شركات أخرى ذات قدرة محدودة أو معدومة على التمويل، إلا أنه كما ذُكر سابقًا، من المرجح أن تؤدي أي عمليات تمويل مصاحبة من جانب شركة بيوديكسا إلى تخفيف حصص الملكية. ويواصل مجلس الإدارة تقييم خيارات التمويل المتاحة للمجموعة، بما في ذلك تلك المرتبطة بالاستحواذ أو الاندماج. وتخضع أي بدائل يتم النظر فيها لموافقة الأطراف المقابلة، وبالتالي، لا يوجد ما يضمن نجاح أي مسار بديل لتمويل الشركة.
يمثل هذا الشرط المتعلق بتمويل إضافي على المدى القصير حالة عدم يقين جوهرية قد تُلقي بظلال من الشك على قدرة المجموعة والشركة الأم على الاستمرار في مزاولة أعمالهما. إذا اتضح في المستقبل عدم وجود خيارات تمويل واقعية متاحة للشركة قبل نفاد مواردها النقدية، فلن تتمكن الشركة من الاستمرار في مزاولة أعمالها. في هذه الحالة، لن نتمكن من إعداد البيانات المالية وفقًا للفقرة 25 من المعيار المحاسبي الدولي رقم 1. وبدلًا من ذلك، سيتم إعداد البيانات المالية على أساس التصفية، وسيتم تقييم الأصول بالقيمة الصافية القابلة للتحقق، وسيتم تسريع استحقاق جميع الالتزامات لتصبح التزامات جارية.
المسائل البيئية، والمجتمع، وقضايا حقوق الإنسان، والموظفين
في 31 ديسمبر 2025، بلغ عدد موظفي المجموعة 11 موظفًا، منهم 4 موظفين يعملون بشكل منتظم في مكاتبها في كارديف. وبناءً على ذلك، تعتقد الشركة أن تأثيرها البيئي محدود نسبيًا. ويحدد دليل الموظفين الخاص بالشركة عددًا من السياسات والإجراءات التي تنظم توقعات المعايير الأخلاقية ومعاملة الموظفين وأصحاب المصلحة الآخرين. كما وضعت الشركة سياسة لمكافحة العبودية وفقًا لقانون مكافحة العبودية الحديثة لعام 2015.
تسعى الشركة جاهدةً لتوفير فرص عمل متكافئة للجميع، بغض النظر عن العرق أو الجنس. في 31 ديسمبر 2025، بلغت نسبة الموظفين الذكور 36% والإناث 64%، ونسبة المديرين التنفيذيين الذكور 57% والإناث 43%، ونسبة أعضاء مجلس الإدارة الذكور 80% والإناث 20%.
الانبعاثات السنوية للغازات الدفيئة
نقيس أداءنا البيئي من خلال الإبلاغ عن بصمتنا الكربونية بوحدة طن مكافئ ثاني أكسيد الكربون. ونقدم تقارير منفصلة عن انبعاثاتنا غير المباشرة الناتجة عن استهلاك الكهرباء (النطاق 2)، والانبعاثات الناتجة عن تنقل الموظفين بسياراتهم لأغراض العمل في المجموعة، والتي تُقدر بناءً على عدد الأميال المقطوعة (النطاق 3). وقد اختارت المجموعة رصد كفاءة استهلاك الطاقة والإبلاغ عنها باستخدام طن ثاني أكسيد الكربون لكل موظف كنسبة كثافة.
المنهجية
عند حساب استهلاك الطاقة المُبلغ عنه وما يعادله من انبعاثات غازات الدفيئة، استندت المجموعة إلى المبادئ التوجيهية لإعداد التقارير البيئية الصادرة عن حكومة المملكة المتحدة وبروتوكول الإبلاغ عن غازات الدفيئة. واستُخدمت منهجية تخصيص قائمة على الموقع لحساب استهلاك الكهرباء.
| أطنان من ثاني أكسيد الكربون | 2025 | 2024 |
| النطاق 2 | 10 | 17 |
| النطاق 3 | 1 | 3 |
| المجموع | 12 | 20 |
| نسبة الكثافة (طن من ثاني أكسيد الكربون لكل موظف) | 1.1 | 0.9 |
بلغت تكاليف الكهرباء للمجموعة لعام 2025 حوالي 16,000 جنيه إسترليني (25,000 جنيه إسترليني في عام 2024). وبلغ استهلاك الطاقة بالكيلوواط/ساعة خلال العام 54,380 كيلوواط/ساعة (81,933 كيلوواط/ساعة في عام 2024). ولا توجد لدى المجموعة خطط فورية لتحسين كفاءة الطاقة.
البيانات المالية الموحدة للدخل الشامل
للسنة المنتهية في 31 ديسمبر
| ملحوظة | 2025 ألف جنيه إسترليني | 2024 ألف جنيه إسترليني | 2023 ألف جنيه إسترليني | |
| ربح | – | – | 381 | |
| دخل آخر | 152 | 31 | 14 | |
| تكاليف البحث والتطوير | (3961) | (5437) | (4067) | |
| التكاليف الإدارية | (4836) | (3793) | (4342) | |
| الخسائر الناجمة عن العمليات | (8645) | (9199) | (8014) | |
| دخل التمويل | 2 | 2385 | 3385 | 570 |
| مصروفات التمويل | 2 | (229) | (165) | (41) |
| الخسارة قبل الضريبة | (6489) | (5979) | (7485) | |
| الضرائب | 105 | 250 | 406 | |
| الخسارة السنوية المنسوبة إلى مالكي الشركة الأم | (6384) | (5729) | (7079) | |
| الدخل الشامل الآخر: | ||||
| البنود التي سيتم أو قد يتم إعادة تصنيفها لاحقاً لتحقيق الربح أو الخسارة: | ||||
| مكاسب الصرف الناتجة عن ترجمة العمليات الأجنبية | 3 | – | – | |
| إجمالي الدخل الشامل الآخر بعد خصم الضرائب | 3 | – | – | |
| إجمالي الخسارة الشاملة المنسوبة إلى مالكي الشركة الأم | (6381) | (5729) | (7079) | |
| خسارة السهم الواحد | ||||
| العمليات المستمرة | ||||
| الخسارة الأساسية والمخففة للسهم العادي - بنس | 3 | (0.01)p | (0.1)p | (2) ص |
تشكل الملاحظات جزءًا لا يتجزأ من هذه البيانات المالية الموحدة.
البيانات المالية الموحدة
في 31 ديسمبر
| رقم الشركة 09216368 | ملحوظة | 2025 ألف جنيه إسترليني | 2024 ألف جنيه إسترليني | 2023 ألف جنيه إسترليني |
| أصول | ||||
| الأصول غير المتداولة | ||||
| الممتلكات والمنشآت والمعدات | 91 | 324 | 571 | |
| الأصول غير الملموسة | 5645 | 5646 | 2941 | |
| 5736 | 5970 | 3512 | ||
| الأصول المتداولة | ||||
| المستحقات التجارية وغيرها | 3786 | 6568 | 637 | |
| مستحقات الضرائب الحالية | 123 | 573 | 422 | |
| النقد وما يعادله | 8534 | 1669 | 5971 | |
| 12443 | 8810 | 7030 | ||
| إجمالي الأصول | 18179 | 14780 | 10,542 | |
| الإلتزامات | ||||
| الالتزامات غير المتداولة | ||||
| النظر المؤجل | 645 | 1306 | – | |
| الاقتراضات | - | 118 | 295 | |
| 645 | 1424 | 295 | ||
| الالتزامات المتداولة | ||||
| المستحقات التجارية وغيرها | 2590 | 3504 | 1240 | |
| النظر المؤجل | 563 | 538 | – | |
| الاقتراضات | 61 | 609 | 169 | |
| الأحكام | - | – | – | |
| الالتزامات المالية المشتقة | 2915 | 383 | 4160 | |
| 6129 | 5034 | 5569 | ||
| إجمالي الالتزامات | 6774 | 6458 | 5864 |
| البيانات المالية الموحدة (تابع) في 31 ديسمبر | ||||
| ملحوظة | 2025 ألف جنيه إسترليني | 2024 ألف جنيه إسترليني | 2023 ألف جنيه إسترليني | |
| رأس المال المصدر والاحتياطيات المنسوبة إلى مالكي الشركة الأم | ||||
| رأس المال | 14,099 | 11,725 | 6253 | |
| علاوة السهم | 98,923 | 93,124 | 86,732 | |
| محمية ميربس | 53003 | 53003 | 53003 | |
| احتياطي الضمان | 1185 | 894 | 3457 | |
| احتياطي النقد الأجنبي | 3 | – | – | |
| العجز المتراكم | (155,808) | (150,424) | (144,767) | |
| إجمالي حقوق الملكية | 11405 | 8322 | 4678 | |
| إجمالي حقوق الملكية والالتزامات | 18179 | 14780 | 10,542 | |
تشكل الملاحظات جزءًا لا يتجزأ من هذه البيانات المالية الموحدة.
البيانات المالية الموحدة للتدفقات النقدية
للسنة المنتهية في 31 ديسمبر
| ملحوظة | 2025 ألف جنيه إسترليني | 2024 ألف جنيه إسترليني | 2023 ألف جنيه إسترليني | |
| التدفقات النقدية من الأنشطة التشغيلية | ||||
| خسائر العام | (6384) | (5729) | (7079) | |
| التعديلات لـ: | ||||
| استهلاك الممتلكات والمنشآت والمعدات | 52 | 117 | 143 | |
| استهلاك أصول حق الاستخدام | 136 | 135 | 137 | |
| استهلاك الأصول الثابتة غير الملموسة | 1 | 2 | 3 | |
| الخسائر الناتجة عن التخلص من الممتلكات والمنشآت والمعدات | 29 | 4 | 2 | |
| انخفاض قيمة القرض | - | – | 79 | |
| انخفاض قيمة الرسوم المقدمة لخط ائتمان خط الائتمان | 373 | - | - | |
| دخل التمويل | (2385) | (3385) | (570) | |
| مصروفات التمويل | 229 | 165 | 41 | |
| رسوم الدفع القائمة على الأسهم | 170 | 283 | 28 | |
| الضرائب | (105) | (250) | (406) | |
| خسائر/أرباح صرف العملات الأجنبية | (130) | 4 | – | |
| التدفقات النقدية من الأنشطة التشغيلية قبل التغيرات في رأس المال العامل | (8014) | (8654) | (7622) | |
| انخفاض/زيادة في الذمم التجارية والمستحقات الأخرى | 2629 | (5975) | 365 | |
| (انخفاض)/زيادة في المستحقات التجارية وغيرها من المستحقات | (913) | 2239 | (207) | |
| (انخفاض) / زيادة في المخصصات | - | – | (207) | |
| النقد المستخدم في العمليات | (6298) | (12390) | (7671) | |
| الضرائب المحصلة | 707 | 129 | 845 | |
| صافي النقد المستخدم في الأنشطة التشغيلية | (5591) | (12261) | (6826) |
البيانات المالية الموحدة للتدفقات النقدية (تابع)
للسنة المنتهية في 31 ديسمبر
| ملحوظة | 2025 ألف جنيه إسترليني | 2024 ألف جنيه إسترليني | 2023 ألف جنيه إسترليني | |
| الأنشطة الاستثمارية | ||||
| شراء الممتلكات والمنشآت والمعدات | (2) | (9) | (26) | |
| عائدات بيع الأصول الثابتة | 18 | – | 4 | |
| شراء أصول غير ملموسة / مقابل مؤجل | (689) | (765) | (237) | |
| تم منح القرض | - | – | (79) | |
| تم تلقي الاهتمام | 90 | 176 | 73 | |
| صافي النقد (المستخدم في) / الناتج عن الأنشطة الاستثمارية | (583) | (598) | (265) | |
| أنشطة التمويل | ||||
| الفائدة المدفوعة | (14) | – | (13) | |
| المبالغ المدفوعة على التزامات الإيجار | (246) | (186) | (188) | |
| (السداد)/عائدات السند الإذني | (450) | 431 | – | |
| أسهم تتضمن سندات قابلة للتحويل، بعد خصم التكاليف | 13749 | 8312 | 10,427 | |
| صافي التدفقات النقدية المتولدة من أنشطة التمويل | 13,039 | 8557 | 10226 | |
| صافي الزيادة/النقصان في النقد وما يعادله | 6865 | (4302) | 3135 | |
| النقد وما يعادله في بداية العام | 1669 | 5971 | 2836 | |
| خسائر/أرباح الصرف على النقد وما يعادله | - | – | – | |
| النقد وما يعادله في نهاية العام | 8534 | 1669 | 5971 |
تشكل الملاحظات جزءًا لا يتجزأ من هذه البيانات المالية الموحدة.
البيانات الموحدة للتغيرات في حقوق الملكية
للسنة المنتهية في 31 ديسمبر
| ملحوظة | يشارك عاصمة ألف جنيه إسترليني | يشارك غالي ألف جنيه إسترليني | محمية ميربس ألف جنيه إسترليني | احتياطي الضمان ألف جنيه إسترليني | احتياطي النقد الأجنبي (بالآلاف من الجنيهات الإسترلينية) | متراكم العجز ألف جنيه إسترليني | المجموع عدالة ألف جنيه إسترليني | |
| في 1 يناير 2025 | 11,725 | 93,124 | 53003 | 894 | – | (150,424) | 8322 | |
| خسائر العام | – | – | – | – | – | (6384) | (6384) | |
| ترجمة العملات الأجنبية | – | – | – | – | 3 | – | 3 | |
| خسارة شاملة كاملة | – | – | – | – | 3 | (6384) | (6381) | |
| المعاملات مع الملاك | ||||||||
| الأسهم الصادرة بموجب اتفاقية ELOC | 2030 | 4817 | – | – | – | – | 6847 | |
| التكاليف المرتبطة باتفاقية ELOC | 86 | (77) | – | – | – | – | 9 | |
| الأسهم المصدرة في 15 مايو 2025 | 100 | 143 | – | – | – | – | 243 | |
| التكاليف المرتبطة بإصدار الأسهم في 15 مايو 2025 | – | (8) | – | – | – | – | (8) | |
| الأسهم المصدرة في 19 ديسمبر 2025 | 158 | 1110 | – | 1184 | – | – | 2452 | |
| التكاليف المرتبطة بإصدار الأسهم في 19 ديسمبر 2025 | – | (186) | – | (173) | – | – | (359) | |
| أوامر القبض المنتهية الصلاحية | – | – | – | (720) | – | 720 | – | |
| رسوم الدفع القائمة على الأسهم | – | – | – | – | – | 280 | 280 | |
| إجمالي مساهمات الملاك وتوزيعات الأرباح عليهم | 2374 | 5799 | 291 | ; border-bottom: solid black 1pt ; text-align: right ; vertical-align: middle; vertical-align: bottom ; "> 1,000 | 9464 | |||
| في 31 ديسمبر 2025 | 14,099 | 98,923 | 53003 | 1185 | 3 | (155,674) | 11405 |
البيانات الموحدة للتغيرات في حقوق الملكية (تابع)
| ملحوظة | يشارك عاصمة ألف جنيه إسترليني | يشارك غالي ألف جنيه إسترليني | محمية ميربس ألف جنيه إسترليني | احتياطي الضمان ألف جنيه إسترليني | متراكم العجز ألف جنيه إسترليني | المجموع عدالة ألف جنيه إسترليني | |
| في 1 يناير 2024 | 6253 | 86,732 | 53003 | 3457 | (144,767) | 4678 | |
| خسائر العام | – | – | – | – | (5729) | (5729) | |
| خسارة شاملة كاملة | – | – | – | – | (5729) | (5729) | |
| المعاملات مع الملاك | |||||||
| الأسهم المصدرة في 22 مايو 2024 | 1614 | 5048 | – | – | – | 6662 | |
| التكاليف المرتبطة بإصدار الأسهم في 22 مايو 2024 | – | (487) | – | – | – | (487) | |
| الأسهم الصادرة في 22 يوليو 2024 | 2105 | 79 | – | 2 | – | 2186 | |
| التكاليف المرتبطة بإصدار الأسهم في 22 يوليو 2024 | – | (55) | – | – | (297) | (352) | |
| ممارسة أوامر الشراء خلال العام | 1602 | 1739 | – | (2565) | – | 776 | |
| إصدار أسهم لشراء أصول غير ملموسة | 151 | 68 | – | – | – | 219 | |
| رسوم الدفع القائمة على الأسهم | – | – | – | – | 369 | 369 | |
| إجمالي مساهمات الملاك وتوزيعات الأرباح عليهم | 5472 | 6392 | – | (2563) | 72 | 9373 | |
| في 31 ديسمبر 2024 | 11,725 | 93,124 | 53003 | 894 | (150,424) | 8322 |
الملاحظات التي تشكل جزءًا من البيانات المالية
للسنة المنتهية في 31 ديسمبر 2025
1. أساس التحضير
أُعدّت البيانات المالية الموحدة وفقًا للمعايير المحاسبية الدولية، بما يتوافق مع متطلبات قانون الشركات لعام 2006، ووفقًا لمعايير إعداد التقارير المالية الدولية. وقد أُعدّت البيانات المالية الموحدة على أساس التكلفة التاريخية، باستثناء الأصول والالتزامات التالية التي تم تقييمها بالقيمة العادلة: بعض الأصول والالتزامات المالية المقاسة بالقيمة العادلة، والالتزامات المتعلقة بالمدفوعات النقدية القائمة على الأسهم.
لا تشكل المعلومات المالية الواردة في هذا الإعلان النهائي بيانات مالية قانونية كما هو محدد في المادة 435 من قانون الشركات لعام 2006. وقد تم استخراج المعلومات المالية من البيانات المالية للسنة المنتهية في 31 ديسمبر 2025 والتي وافق عليها مجلس الإدارة، وتستند الأرقام المقارنة للسنتين المنتهيتين في 31 ديسمبر 2024 و31 ديسمبر 2023 إلى البيانات المالية لتلك السنة.
تم تسليم البيانات المالية لعامي 2024 و2023 إلى مسجل الشركات، وسيتم تسليم البيانات المالية لعام 2025 بعد الاجتماع العام السنوي.
جاء تقرير مدقق الحسابات الخاص بالتقرير السنوي والحسابات للشركة لعام 2025 دون تحفظات، ولكنه أشار إلى وجود شكوك جوهرية تتعلق باستمرارية الشركة. ولم يتضمن تقرير مدقق الحسابات أي بيانات بموجب المادة 498 (2) أو (3) من قانون الشركات لعام 2006.
على الرغم من أن المعلومات المالية الواردة في هذا الإعلان عن النتائج قد أُعدت وفقًا للمعايير الدولية لإعداد التقارير المالية (IFRS)، إلا أن هذا الإعلان لا يحتوي في حد ذاته على معلومات كافية للامتثال لهذه المعايير. وقد وافق مجلس الإدارة على المعلومات الواردة في هذا الإعلان عن النتائج بتاريخ 27 مارس 2026.
استمرارية العمل – عدم اليقين المادي
تكبدت المجموعة والشركة خسائر صافية وتدفقات نقدية خارجة كبيرة من النقد المستخدم في الأنشطة التشغيلية خلال السنوات الماضية في إطار تطوير محفظتها الاستثمارية. وفي السنة المنتهية في 31 ديسمبر 2025، تكبدت المجموعة خسارة موحدة قدرها 6.38 مليون جنيه إسترليني وتدفقات نقدية سلبية من العمليات التشغيلية قدرها 5.59 مليون جنيه إسترليني. وبلغ العجز المتراكم للمجموعة في 31 ديسمبر 2025 مبلغ 155.81 مليون جنيه إسترليني.
يعتمد استمرار المجموعة في المستقبل على قدرتها على جمع السيولة من خلال أنشطة التمويل لتمويل خططها التنموية إلى حين تحقيق مراحل محددة و/أو الحصول على عوائد من شراكاتها في أصول الشركة. وقد يؤدي عجز المجموعة عن جمع رأس المال عند الحاجة إلى تأثير سلبي على وضعها المالي وقدرتها على تنفيذ استراتيجياتها التجارية.
يرى مجلس الإدارة أن هناك خيارات كافية ووقتًا مناسبًا لتأمين تمويل إضافي للشركة، وبعد دراسة أوجه عدم اليقين، يرى المجلس أنه من المناسب الاستمرار في اعتماد مبدأ استمرارية النشاط في إعداد هذه البيانات المالية. ولذلك، عُرضت البيانات المالية الموحدة للمجموعة على أساس استمرارية النشاط، والذي يأخذ في الاعتبار تحقيق الأصول وسداد الالتزامات في سياق العمل المعتاد.
في 31 ديسمبر 2025، بلغ رصيد المجموعة من النقد وما يعادله 8.53 مليون جنيه إسترليني. وقد أعدّ مجلس الإدارة توقعات التدفقات النقدية، ودرس احتياجات المجموعة من التدفقات النقدية للسنوات الثلاث المقبلة، بما في ذلك فترة الاثني عشر شهرًا من تاريخ اعتماد البيانات المالية الموحدة. وتشير هذه التوقعات إلى الحاجة إلى تمويل إضافي في الربع الثالث من عام 2026، بافتراض، من بين أمور أخرى، استمرار بعض برامج التطوير والأنشطة التشغيلية الأخرى وفقًا للخطة الحالية. وبموجب خط ائتمان حقوق الملكية البالغ 35 مليون دولار أمريكي، كما هو موضح في مراجعة الشؤون المالية، يجوز للشركة توجيه شركة C/M لشراء أسهم الإيداع الأمريكية (مع مراعاة بعض القيود) واستلام العائدات وفقًا لسعر محدد. ولا يوجد ما يضمن قدرة الشركة على استخدام خط ائتمان حقوق الملكية أو الحصول على تمويل من مصادر أخرى بالقدر اللازم لتمويل عملياتها. وفي 31 ديسمبر 2025، لا يزال مبلغ 26.08 مليون دولار أمريكي غير مسحوب من خط ائتمان حقوق الملكية.
يرى مجلس الإدارة أن بيئة تمويل شركات التكنولوجيا الحيوية الصغيرة والمتناهية الصغر لا تزال مليئة بالتحديات. ورغم أن هذا قد يتيح فرصًا للاستحواذ أو الاندماج مع شركات أخرى ذات قدرة محدودة أو معدومة على التمويل، إلا أنه كما ذُكر سابقًا، من المرجح أن تؤدي أي عمليات تمويل مصاحبة من جانب شركة بيوديكسا إلى تخفيف حصص الملكية. ويواصل مجلس الإدارة تقييم خيارات التمويل المتاحة للمجموعة، بما في ذلك تلك المرتبطة بالاستحواذ أو الاندماج. وتخضع أي بدائل يتم النظر فيها لموافقة الأطراف المقابلة، وبالتالي، لا يوجد ما يضمن نجاح أي مسار بديل لتمويل الشركة.
يمثل هذا الشرط المتعلق بتمويل إضافي على المدى القصير حالة عدم يقين جوهرية قد تُلقي بظلال من الشك على قدرة المجموعة والشركة الأم على الاستمرار في مزاولة أعمالهما. إذا اتضح في المستقبل عدم وجود خيارات تمويل واقعية متاحة للشركة قبل نفاد مواردها النقدية، فلن تتمكن الشركة من الاستمرار في مزاولة أعمالها. في هذه الحالة، لن نتمكن من إعداد البيانات المالية وفقًا للفقرة 25 من المعيار المحاسبي الدولي رقم 1. وبدلًا من ذلك، سيتم إعداد البيانات المالية على أساس التصفية، وسيتم تقييم الأصول بالقيمة الصافية القابلة للتحقق، وسيتم تسريع استحقاق جميع الالتزامات لتصبح التزامات جارية.
المحاسبة عن منحة rRapa و CPRIT
في 25 أبريل 2024، أبرمت الشركة اتفاقية ترخيص وتعاون مع شركة راباميسين هولدينغز (المعروفة تجارياً باسم إمتورا بيوساينسز). وتتوافق اتفاقية الترخيص والتعاون المبرمة مع إمتورا مع تعريف الترتيب المشترك بموجب المعيار الدولي لإعداد التقارير المالية 11، وتحديداً فيما يتعلق ببرنامج FAP.
تم إنشاء حساب ضمان مشترك عند إتمام اتفاقية دورة حياة المنتج (LCA). تُعالج معاملات برنامج FAP المؤهلة للتخصيص مقابل منحة CPRIT والتمويل المُطابق من خلال حساب الضمان، بما في ذلك إيداعات الشركة للأموال المُطابقة، كما هو مُبين في الاتفاقية، واستلام تمويل المنحة من CPRIT، ودفع نفقات البحث والتطوير المؤهلة. على الرغم من أن منحة CPRIT وعقود موردي البحث والتطوير مُبرمة مع شركة إمتورا، إلا أن طبيعة الترتيب المشترك لاتفاقية دورة حياة المنتج (LCA) تجعل إمتورا تُعتبر وكيلاً للشركة. وبناءً على ذلك، تُسجل الشركة 100% من المنحة و100% من نفقات البحث والتطوير. يتم تسجيل منحة CPRIT على أساس مُطابقة 1:2 لأول 17 مليون دولار، بينما يتم تسجيل آخر 3 ملايين دولار على أساس 1:1. ووفقًا للسياسة المحاسبية للشركة، تُقيد المنحة، باعتبارها سدادًا للتكاليف ذات الصلة المباشرة، ضمن تكاليف البحث والتطوير في نفس الفترة في بيانات الدخل الشامل. يتم الاعتراف بحساب الضمان ضمن المدفوعات المسبقة، ويتم الاعتراف بمنحة CPRIT المستلمة مقدماً ضمن الإيرادات المؤجلة، ويتم الاعتراف بأي منحة لم يتم استلامها بعد ضمن الإيرادات المستحقة.
كانت الأرصدة كما في 31 ديسمبر على النحو التالي فيما يتعلق بمشروع FAP:
| 31 ديسمبر 2025 ألف جنيه إسترليني | 31 ديسمبر 2024 ألف جنيه إسترليني | |
| الدفعات المسبقة* | 2842 | 6114 |
| الإيرادات المؤجلة | 571 | 1468 |
* الدفعة المقدمة تعكس فقط رصيد حساب الضمان
2. الإيرادات والمصروفات المالية
| 2025 ألف جنيه إسترليني | 2024 ألف جنيه إسترليني | 2023 ألف جنيه إسترليني | |
| دخل التمويل | |||
| الفوائد المحصلة على الودائع المصرفية | 83 | 166 | 73 |
| فوائد أخرى مستحقة | 6 | 1 | 10 |
| الربح من الأسهم المسددة من الالتزامات المالية المشتقة | 2296 | 3218 | 487 |
| إجمالي دخل التمويل | 2385 | 3385 | 570 |
| 2025 ألف جنيه إسترليني | 2024 ألف جنيه إسترليني | 2023 ألف جنيه إسترليني | |
| مصروفات التمويل | |||
| مصروفات الفائدة على التزامات الإيجار | 10 | 19 | 28 |
| مصروفات الفائدة على المقابل المؤجل | 159 | 144 | – |
| قروض أخرى | 60 | 2 | 13 |
| إجمالي المصاريف المالية | 229 | 165 | 41 |
3. خسارة السهم الواحد
| 2025 ألف جنيه إسترليني | 2024 ألف جنيه إسترليني | 2023 ألف جنيه إسترليني | |
| البسط | |||
| الخسائر المستخدمة في حساب ربحية السهم الأساسية وربحية السهم المخففة: | |||
| العمليات المستمرة | (6384) | (5729) | (7079) |
| المقام | |||
| متوسط عدد الأسهم العادية المرجح المستخدم في حساب ربحية السهم الأساسية: | 54,861,066,264 | 4,952,784,179 | 315,849,600 |
| الخسارة الأساسية والمخففة للسهم الواحد: | |||
| العمليات المستمرة - بنسات | (0.01)p | (0.1)p | (2) ص |
في اجتماع الجمعية العمومية المنعقد في 1 يونيو 2025، وافق المساهمون على تقسيم وإعادة تصنيف أسهم الشركة العادية المصدرة، بقيمة 0.00005 جنيه إسترليني للسهم الواحد، إلى سهم عادي واحد بقيمة 0.000001 جنيه إسترليني و49 سهمًا مؤجلًا من الفئة "د" بقيمة 0.000001 جنيه إسترليني للسهم الواحد. تتمتع الأسهم المؤجلة من الفئة "د" بحقوق محدودة، وهي عمليًا بلا قيمة. لم يؤثر تقسيم الأسهم وإعادة تصنيفها على حساب المقام، حيث لم يتغير عدد الأسهم العادية المصدرة.
أصدرت الشركة خلال العام سندات تم احتسابها من خلال احتياطي السندات.
أخذت الشركة في الاعتبار الإرشادات الواردة في المعيار المحاسبي الدولي رقم 33 عند حساب المقام فيما يتعلق بإصدار سندات الشراء الممولة مسبقًا. وقد أقرت الإدارة هذه السندات من تاريخ منحها وليس من تاريخ إصدار الأسهم العادية المقابلة عند حساب المقام.
تكبدت المجموعة خسارة في الفترتين الحالية والسابقة المعروضتين، ولذلك فإن خيارات الأسهم وحقوق الشراء لا تُخفف من قيمة السهم. ونتيجة لذلك، يتم عرض الخسارة المخففة للسهم الواحد على نفس أساس الخسارة الأساسية للسهم الواحد.
4. رأس المال المدفوع
| مصرح به، ومخصص بالكامل مدفوع – مصنف كحقوق ملكية | 2025 رقم | 2025 جنيه إسترليني | 2024 رقم | 2024 جنيه إسترليني | 2023 رقم | 2023 جنيه إسترليني |
| في 31 ديسمبر | ||||||
| الأسهم العادية لـ 0.000001 جنيه إسترليني لكل منها | 225,817,808,922 | 225,818 | 6,685,918,922 | 334,296 | 1,189,577,722 | 1,189,578 |
| أسهم مؤجلة من الفئة "أ" بقيمة جنيه إسترليني واحد للسهم الواحد | 1,000,001 | 1,000,001 | 1,000,001 | 1,000,001 | 1,000,001 | 1,000,001 |
| أسهم مؤجلة من الفئة "ب" بقيمة 0.001 جنيه إسترليني للسهم الواحد | 4,063,321,418 | 4,063,321 | 4,063,321,418 | 4,063,321 | 4,063,321,418 | 4,063,321 |
| أسهم مؤجلة من الفئة "ج" بقيمة 0.00005 جنيه إسترليني للسهم الواحد | 126,547,389,518 | 6,327,370 | 126,547,389,518 | 6,327,370 | – | – |
| أسهم مؤجلة من الفئة "د" بقيمة 0.000001 جنيه إسترليني للسهم الواحد | 2,482,747,137,178 | 2,482,747 | – | – | – | – |
| المجموع | 14,099,257 | 11,724,988 | 6,252,900 |
في اجتماع الجمعية العمومية المنعقد بتاريخ 11 يونيو 2025، وافق المساهمون على تقسيم وإعادة تصنيف أسهم الشركة العادية المصدرة، بقيمة 0.00005 جنيه إسترليني للسهم الواحد، إلى سهم عادي واحد بقيمة 0.000001 جنيه إسترليني و49 سهمًا مؤجلًا من الفئة "د" بقيمة 0.000001 جنيه إسترليني للسهم الواحد. تتمتع الأسهم المؤجلة من الفئة "د" بحقوق محدودة، وهي عمليًا عديمة القيمة.
في 31 يوليو 2025، أجرت الشركة تغييرًا في نسبة عدد الأسهم العادية الممثلة بشهادات الإيداع الأمريكية من 10000 سهم عادي لكل شهادة إيداع أمريكية إلى 100000 سهم عادي لكل شهادة إيداع أمريكية.
وفقًا للنظام الأساسي للشركة المعتمد في 11 يونيو 2025، يتكون رأس مال الشركة من عدد غير محدود من الأسهم العادية بقيمة اسمية قدرها 0.000001 جنيه إسترليني للسهم الواحد. وقد سُجلت الأسهم العادية والمؤجلة كحقوق ملكية.
5. معاملات الأطراف ذات العلاقة
يرى أعضاء مجلس الإدارة أنه لا توجد معاملات مع أطراف ذات صلة خلال الفترات المبلغ عنها باستثناء مكافآت أعضاء مجلس الإدارة.
6. الأحداث التي وقعت بعد تاريخ الإبلاغ
في 4 فبراير 2026، أعلنت الشركة أنها أبرمت اتفاقية ترخيص وتعاون ("اتفاقية الترخيص") مع شركة أوتسوكا للأدوية المحدودة ("أوتسوكا")، وبموجبها منحت أوتسوكا الشركة ترخيصًا حصريًا عالميًا (باستثناء اليابان) ("المنطقة المرخصة") لتطوير وتصنيع وتسويق OPB-171755، والذي سيُطلق عليه اسم MTX240 ("MTX240")، وهو مرشح علاجي جزيئي لاصق جاهز للمرحلة الأولى، لجميع الاستخدامات العلاجية البشرية. تعتزم الشركة في البداية تطوير عقار MTX240 لعلاج أورام اللحمة المعدية المعوية.
بموجب اتفاقية الترخيص، ستكون الشركة مسؤولة عن جميع أنشطة التطوير والتصنيع والتسويق لمنتج MTX240 في المنطقة المرخصة، وستحتفظ شركة أوتسوكا بجميع حقوق MTX240 في اليابان. وقد دفعت الشركة مبلغًا مقدمًا لأوتسوكا مقابل الترخيص، وتستحق أوتسوكا الحصول على عوائد لمرة واحدة عند تحقيق مراحل التطوير والموافقات التنظيمية، بالإضافة إلى عوائد متدرجة بنسبة تتراوح بين 5% و9% من صافي مبيعات المنتجات المرخصة. كما تلتزم الشركة بدفع نسبة مئوية من أي دخل تحصل عليه أوتسوكا من التراخيص الفرعية، مع مراعاة بعض الاستثناءات.
في 18 مارس 2026، أعلنت الشركة عن تغيير في نسبة أسهمها العادية من كل إيصال إيداع أمريكي يمثل 100,000 سهم عادي إلى كل إيصال إيداع أمريكي يمثل 500,000 سهم عادي.

