أعلنت شركة سينتي بيوساينسز هولدينغز عن اجتماع إيجابي مع لجنة مراجعة الأدوية التابعة لإدارة الغذاء والدواء الأمريكية (FDA RMAT) بشأن استراتيجية التسجيل السريري واستراتيجية التصنيع والتحكم (CMC) لعقار سينتي-202 لعلاج ابيضاض الدم النخاعي الحاد (AML) ...
Senti Biosciences Holdings Inc SNTI | 0.00 |
بعد اجتماع من النوع "ب" مع إدارة الغذاء والدواء الأمريكية، تخطط شركة سينتي بايو للمضي قدمًا في تجربة تسجيلية متعددة المراكز أحادية الذراع لعقار سينتي-202، استنادًا إلى النتائج السريرية القوية للمرحلة الأولى التي أظهرت حالات شفاء كاملة عميقة ومستدامة خالية من الحد الأدنى من المرض المتبقي.
لزيادة تحسين فعالية SENTI-202، ستتضمن معايير اختيار المتبرعين لجميع عمليات التصنيع المستقبلية النمط الظاهري "المتبرع X".
حقق المرضى في المرحلة الأولى من التجارب السريرية الذين تلقوا SENTI-202 من الخلايا القاتلة الطبيعية المشتقة من المتبرع X معدل استجابة كاملة مركبة (cCR) بنسبة 50%
جنوب سان فرانسيسكو، كاليفورنيا، 14 مايو 2026 (جلوب نيوزواير) - أعلنت شركة Senti Biosciences Holdings, Inc. (ناسداك: SNTI) ("Senti Bio" أو "الشركة")، وهي شركة للتكنولوجيا الحيوية في المرحلة السريرية تعمل على تطوير علاجات الخلايا والجينات من الجيل التالي باستخدام منصة Gene Circuit الخاصة بها، اليوم عن إتمامها بنجاح اجتماعًا أوليًا شاملًا متعدد التخصصات من النوع B للعلاج المتقدم للطب التجديدي (RMAT) مع إدارة الغذاء والدواء الأمريكية (FDA) بشأن SENTI-202، وهو أول علاج من نوعه للشركة بتقنية الخلايا CAR-NK الجاهزة للاستخدام والمعتمدة على Logic Gated لعلاج سرطان الدم النخاعي الحاد المتكرر/المقاوم (R/R AML) وبيانات المرحلة الأولى السريرية المحدثة.
عقب اجتماع لجنة مراجعة الأدوية، وضعت الشركة اللمسات الأخيرة على استراتيجيتها السريرية المحورية واستراتيجيتها المتعلقة بالكيمياء والتصنيع والرقابة (CMC) لعقار SENTI-202. وتعتزم الشركة تنفيذ تجربة سريرية محورية متعددة المراكز ذات ذراع واحد، تهدف إلى دعم تسجيل عقار SENTI-202 المحتمل لدى مرضى ابيضاض الدم النخاعي الحاد المقاوم للعلاج أو المتكرر. ومن المتوقع أن تقيّم هذه الدراسة عقار SENTI-202 عند إعطائه بعد العلاج الكيميائي المُثبِّط للخلايا اللمفاوية، وذلك لدى مجموعة من المرضى تتوافق مع مجموعة المرضى المشاركين في المرحلة الأولى من التجارب السريرية.
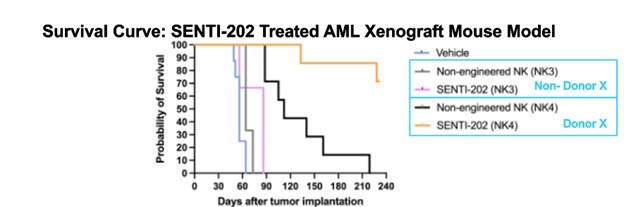
بالإضافة إلى الاجتماع الإيجابي للجنة مراجعة العلاج الإشعاعي (RMAT)، وبعد إجراء تحليل استكشافي لفعالية المتغيرات المصاحبة لنتائج المرحلة الأولى من التجارب السريرية، حددت شركة سينتي سمة محددة للمتبرع X ترتبط بفعالية دواء سينتي-202، حيث حقق 50% من المرضى (7 من 14) استجابة سريرية كاملة (cCR) عند تلقيهم أي جرعات من سينتي-202 المصنعة من خلايا NK المشتقة من المتبرع X في الدورة الأولى، مقابل 12.5% فقط (1 من 8) ممن حققوا استجابة سريرية كاملة عند تلقيهم سينتي-202 المصنع من خلايا NK غير المشتقة من المتبرع X (انظر الجدول أدناه). ونتيجةً لهذا الاكتشاف، سيُستخدم المتبرع X في جميع عمليات تصنيع سينتي-202 المستقبلية، بما في ذلك استخدامها في الدراسات المحورية. وتوجد سمة المتبرع X لدى حوالي 50% من المتبرعين البالغين، وتؤكد الدراسات المنشورة زيادة سمية خلايا NK لدى المتبرعين الذين يحملون هذه السمة. لا يعتمد النمط الظاهري للخلايا القاتلة الطبيعية من المتبرع X على تطابق مستضدات الكريات البيضاء البشرية (HLA) أو مستقبلات الكير (KIR)، مما يدعم استخدام SENTI-202 الجاهز للاستخدام في عمليات زرع الخلايا الجذعية من متبرعين آخرين. وقد أكد التحليل الاسترجاعي لبيانات نموذج الفئران MV4-11 NSG قبل السريرية زيادة النشاط والبقاء على قيد الحياة مع منتج المتبرع X (انظر الشكل أدناه).
أعلنت شركة سينتي بايو أيضًا أن عقار SENTI-202 لا يزال يُظهر استجابات مستدامة وخالية من المرض المتبقي (MRD) في المرحلة الأولى من التجارب السريرية التي شملت 22 مريضًا، وهو ما يُقارن بشكل إيجابي مع العلاجات الحالية المعتمدة من إدارة الغذاء والدواء الأمريكية لسرطان الدم النخاعي الحاد المقاوم للعلاج أو المتكرر. عند الوصول إلى الجرعة الموصى بها للمرحلة الثانية (RP2D)، لوحظ معدل استجابة إجمالي (ORR) بنسبة 44% ومعدل استجابة كاملة سريرية (cCR) بنسبة 37.5% لدى جميع المرضى الذين تلقوا مزيجًا من مواد من متبرع X ومواد من غير متبرع X، مع كون جميع حالات الاستجابة الكاملة خالية من المرض المتبقي. ولا تزال حالات الاستجابة الكاملة مستدامة، حيث استمر جميع المرضى الذين استجابوا لحالات الاستجابة الكاملة/الاستجابة الكاملة مع استئصال جزئي للنخاع العظمي (CR/CRh) والذين كانوا في حالة هدأة عند جمع البيانات التي تدعم العرض الشفهي في الاجتماع السنوي لجمعية أمراض الدم الأمريكية (ASH) لعام 2025، في الحفاظ على حالة الهدأة مع متابعة إضافية لمدة 7 أشهر، وكانت أطول مدة متابعة 21 شهرًا أو أكثر.
"يمثل هذا الاجتماع الإيجابي مع لجنة مراجعة الأدوية المعتمدة من إدارة الغذاء والدواء الأمريكية (FDA RMAT) لحظةً فارقةً لشركة سينتي بايو، ويُعزز بشكلٍ كبيرٍ مسارنا نحو التسجيل المحتمل لعقار SENTI-202"، صرّح بذلك الدكتور تيم لو، الرئيس التنفيذي والمؤسس المشارك لشركة سينتي بايو. وأضاف: "هذا الخبر، إلى جانب الاستجابات السريرية الواعدة التي لوحظت حتى الآن والتي أدت إلى تحسينات في استراتيجية اختيار المتبرعين لدينا، يُؤهلنا للمضي قدمًا بعقار SENTI-202 نحو دراسة تسجيل محتملة لعلاج ابيضاض الدم النخاعي الحاد المُنتكس/المُقاوم للعلاج. ونعتقد أن هذا الإنجاز يُعزز من صحة منصة الدوائر الجينية الخاصة بنا، والإمكانات العلاجية المتميزة لعلاجات الخلايا المُعتمدة على البوابات المنطقية."
سبق أن منحت إدارة الغذاء والدواء الأمريكية (FDA) تصنيف RMAT لـ SENTI-202. ويهدف هذا البرنامج إلى تسهيل التطوير والمراجعة السريعة لعلاجات الطب التجديدي التي تعالج الأمراض الخطيرة أو المهددة للحياة.
"تُقدّم ملاحظات إدارة الغذاء والدواء الأمريكية توضيحًا هامًا لاستراتيجيتنا التطويرية للتسجيل، وتُعزّز ثقتنا ببرنامج SENTI-202"، صرّحت بذلك الدكتورة كانيا راجانجام، الحاصلة على شهادتيّ الطب والدكتوراه، كبيرة المسؤولين الطبيين في شركة Senti Bio. وأضافت: "إنّ النشاط السريري الممتاز الذي لوحظ حتى الآن، بما في ذلك حالات الشفاء التام والمستدام مع سلبية الحد الأدنى من المرض المتبقي، إلى جانب سجلّ السلامة الجيد، يمنحنا الثقة ونحن ننتقل إلى المراحل اللاحقة من التطوير. نحن نركّز على التنفيذ السريع للدراسة المحورية، مع استكشاف فرص التوسع المحتملة في حالات ابيضاض الدم النخاعي الحاد المُشخّصة حديثًا وابيضاض الدم النخاعي الحاد لدى الأطفال. منذ تقديم طلبنا للحصول على ترخيص دواء جديد (IND)، ركّزت Senti على اختيار المتبرعين لتقليل التباين. نحن في وضع قويّ ونحن نستعد لتجاربنا السريرية، وذلك بفضل تحديد نمط ظاهري للمتبرع يرتبط بزيادة النشاط، ويستمر في دعم تصنيع SENTI-202 من متبرعين غير متطابقين."
لا يزال سرطان الدم النخاعي الحاد المتكرر/المقاوم للعلاج ورمًا خبيثًا دمويًا عدوانيًا ذو خيارات علاجية محدودة ونتائج بقاء ضعيفة على المدى الطويل. وتعتقد شركة سينتي بايو أن آلية عمل دواء SENTI-202 المتميزة، وتوافره الجاهز للاستخدام، ونتائجه السريرية المبكرة الواعدة، تجعل منه خيارًا علاجيًا مهمًا محتملًا من الجيل التالي لمرضى سرطان الدم النخاعي الحاد.
| جدول: بيانات فعالية المرحلة الأولى من تجربة SENTI-202-101 لمرضى ابيضاض الدم النخاعي الحاد المقاوم/الناكس بناءً على المتبرع النمط الظاهري | ||
| جميع المرضى (عدد المشاركين = 22 ) | أي متبرع X في الدورة 1 | لا يوجد متبرع X في الدورة 1 |
| معدل الاستجابة الإجمالي (ORR) | 8/14 (57%) | 2/8 (25%) |
| cCR | 7/14 (50%) | 1/8 (12.5%) |
| عربة | غير مُهندس NK (NK3) | SENTI-202 (NK3) | غير مُهندس NK (NK4) | SENTI-202 (NK4) | |
| متوسط البقاء على قيد الحياة (يوم) | 56.0 | 64.0 | 86.0 | 112.0 | لم يتم الوصول إليه |
| الشكل: يؤكد التحليل الاسترجاعي لبيانات نموذج الفأر MV4-11 NSG قبل السريرية زيادة النشاط والبقاء على قيد الحياة مع SENTI-202 مصنوع من منتج المتبرع X. تم تأكيد خصائص المتبرع X لاحقاً. | |||||
حول SENTI-202
يُعدّ SENTI-202 علاجًا رائدًا من نوعه، مُصمّمًا بتقنية الخلايا القاتلة الطبيعية المُعدّلة وراثيًا (CAR-NK)، ويستهدف بشكل انتقائي الأورام الدموية الخبيثة التي تُعبّر عن CD33 و/أو FLT3، بما في ذلك ابيضاض الدم النخاعي الحاد (AML) ومتلازمة خلل التنسج النخاعي (MDS)، ويقضي عليها، مع الحفاظ على خلايا نخاع العظم السليمة. يحتوي SENTI-202 على دوائر جينية مُهندسة متعددة، تشمل أنظمة منطقية OR GATE وNOT GATE، بالإضافة إلى إطلاق مُعاير للإنترلوكين-15 (IL-15)، لتحسين استهداف الورم، واستمراريته، وفعاليته العلاجية.
حصل دواء SENTI-202 على تصنيف العلاج المتقدم للطب التجديدي (RMAT) وتصنيف الدواء اليتيم (ODD) من إدارة الغذاء والدواء الأمريكية.
حول دراسة المرحلة الأولى
تضمنت الدراسة متعددة الجنسيات ومتعددة المراكز لتحديد الجرعة لـ SENTI-202 ( NCT06325748 ) تحديد الجرعة الأولية باستخدام تصميم دراسة "3+3" المعدل لتحديد الجرعة القصوى المسموح بها (MTD) و/أو الجرعة الموصى بها للمرحلة الثانية (RP2D) من SENTI-202 عند إعطائها بعد العلاج الكيميائي المستنفد للخلايا اللمفاوية (الجزء 1) متبوعًا بمجموعات توسع خاصة بالمرض عند RP2D (الجزء 2).
تمثلت الأهداف الرئيسية في تقييم السلامة، وتحديد الجرعة القصوى المسموح بها (MTD) والجرعة الموصى بها للمرحلة الثانية (RP2D)، وتقييم الفعالية في مجموعات التوسع باستخدام معايير ELN 2022 المتفق عليها لسرطان الدم النخاعي الحاد (AML)، مع أهداف ثانوية رئيسية تشمل تقييم المرض المتبقي القابل للقياس، والحركية الدوائية، والديناميكية الدوائية باستخدام تقنية CyTOF على عينات متسلسلة من نخاع العظم. لمزيد من المعلومات، تفضل بزيارة clinicaltrials.gov .
نبذة عن سنتي بايو
شركة سينتي بايو هي شركة للتكنولوجيا الحيوية في المرحلة السريرية، تعمل على تطوير جيل جديد من العلاجات الخلوية والجينية للمرضى الذين يعانون من أمراض مستعصية. ولتحقيق ذلك، تستفيد سينتي بايو من منصتها في علم الأحياء التركيبي لهندسة الدوائر الجينية في أدوية جديدة تتميز بدقة وتحكم مُحسّنين. صُممت هذه الدوائر الجينية للقضاء بدقة على الخلايا السرطانية، والحفاظ على الخلايا السليمة، وزيادة التخصص في استهداف الأنسجة، و/أو إمكانية التحكم بها حتى بعد إعطائها. تتضمن مجموعة منتجات الشركة، المملوكة بالكامل، علاجات خلوية مُهندسة باستخدام الدوائر الجينية لاستهداف مؤشرات الأورام السائلة والصلبة الصعبة. وقد أظهرت الدراسات قبل السريرية فعالية الدوائر الجينية لشركة سينتي بايو في كل من الخلايا القاتلة الطبيعية والخلايا التائية. كما أثبتت سينتي بايو، من خلال دراسات قبل السريرية، النطاق الواسع المحتمل للدوائر الجينية في طرق علاجية وأمراض أخرى خارج نطاق الأورام، وتواصل تطوير هذه القدرات من خلال الشراكات.
البيانات التطلعية
يحتوي هذا البيان الصحفي وهذه الوثيقة على بعض التصريحات التي لا تُعدّ حقائق تاريخية، وتُعتبر تصريحات استشرافية بالمعنى المقصود في المادة 27أ من قانون الأوراق المالية لعام 1933، بصيغته المعدلة، والمادة 21هـ من قانون سوق الأوراق المالية لعام 1934، بصيغته المعدلة. ويمكن تمييز هذه التصريحات الاستشرافية عمومًا من خلال كلمات مثل "نعتقد"، "قد"، "نتوقع"، "نستمر"، "جاري"، "نخطط"، "نتوقع"، "نتنبأ"، "نقدر"، "ننوي"، "استراتيجية"، "مستقبل"، "فرصة"، "خطة"، "ربما"، "ينبغي"، "سوف"، "سيكون"، "سيستمر"، "من المرجح أن ينتج عنه"، "نتوقع"، "نسعى"، "نستهدف"، وتعبيرات مشابهة تتنبأ أو تشير إلى أحداث أو اتجاهات مستقبلية، أو لا تُعدّ تصريحات تتعلق بوقائع تاريخية. البيانات التطلعية هي تنبؤات وتوقعات وتصريحات أخرى حول أحداث مستقبلية تستند إلى التوقعات الحالية لإدارة شركة سنتي بايو وافتراضاتها، سواء أكانت مذكورة في هذه الوثيقة أم لا، وبالتالي فهي عرضة للمخاطر والشكوك. تشمل البيانات التطلعية، على سبيل المثال لا الحصر، التوقعات المتعلقة بنتائج سنتي بايو المستقبلية. تُقدم هذه البيانات التطلعية لأغراض توضيحية فقط، ولا يُقصد بها أن تكون بمثابة ضمان أو تأكيد أو تنبؤ أو بيان قاطع لحقيقة أو احتمال، ولا يجوز لأي مستثمر الاعتماد عليها في هذا الشأن. يصعب أو يستحيل التنبؤ بالأحداث والظروف الفعلية، وستختلف عن الافتراضات. العديد من الأحداث والظروف الفعلية خارجة عن سيطرة سنتي بايو. قد تؤدي عوامل عديدة إلى اختلاف النتائج المستقبلية الفعلية اختلافًا جوهريًا عن البيانات التطلعية الواردة في هذه الوثيقة، بما في ذلك على سبيل المثال لا الحصر: (1) التغيرات في ظروف الأعمال والأسواق والظروف المالية والسياسية والقانونية المحلية والأجنبية، (2) التغيرات في الصناعات التنافسية والخاضعة لتنظيمات صارمة التي تعمل فيها شركة سنتي بايو، والاختلافات في الأداء التشغيلي بين المنافسين، والتغيرات في القوانين واللوائح التي تؤثر على أعمال سنتي بايو، (3) القدرة على تنفيذ خطط العمل والتوقعات وغيرها من التوقعات، (4) مخاطر الانكماش وتغير البيئة التنظيمية في صناعة سنتي بايو شديدة التنافسية، (5) المخاطر المتعلقة بعدم اليقين بشأن أي معلومات مالية متوقعة فيما يتعلق بشركة سنتي بايو، (6) المخاطر المتعلقة بعدم اليقين بشأن توقيت أو نتائج الدراسات السريرية لشركة سنتي بايو، وتسجيل المرضى، وأنشطة بدء التصنيع وفقًا لممارسات التصنيع الجيدة، (7) اعتماد شركة سنتي بايو على أطراف ثالثة فيما يتعلق بالدراسات السريرية وأنشطة التصنيع وفقًا لممارسات التصنيع الجيدة، (8) المخاطر المتعلقة بالتأخيرات والتأثيرات الأخرى الناجمة عن الأحداث الاقتصادية الكلية والجيوسياسية، وارتفاع معدلات التضخم، وارتفاع أسعار الفائدة على العمليات التجارية، (9) المخاطر المتعلقة بتوقيت واستخدام المنحة المقدمة من معهد كاليفورنيا للطب التجديدي (CIRM)، و(x) نجاح أي جهود بحثية وتطويرية مستقبلية تقوم بها شركة سنتي بايو. القائمة السابقة للعوامل ليست شاملة. يجب عليكم دراسة العوامل المذكورة أعلاه والمخاطر والشكوك الأخرى الموضحة في قسم "عوامل الخطر" من أحدث تقرير سنوي لشركة سنتي بايو المُقدم إلى هيئة الأوراق المالية والبورصات الأمريكية ("SEC")، والوثائق الأخرى التي تقدمها سنتي بايو من حين لآخر إلى الهيئة، بعناية. تُحدد هذه الإفصاحات وتتناول مخاطر وشكوكًا أخرى مهمة قد تؤدي إلى اختلاف الأحداث والنتائج الفعلية اختلافًا جوهريًا عن تلك الواردة في البيانات التطلعية في هذه الوثيقة. قد تكون هناك مخاطر إضافية لا تعرفها سنتي بايو حاليًا، أو تعتقد سنتي بايو حاليًا أنها غير جوهرية، والتي قد تؤدي أيضًا إلى اختلاف النتائج الفعلية عن تلك الواردة في البيانات التطلعية في هذه الوثيقة. البيانات التطلعية صحيحة فقط اعتبارًا من تاريخ إصدارها. تتوقع سنتي بايو أن الأحداث والتطورات اللاحقة قد تؤدي إلى تغيير تقييماتها. باستثناء ما يقتضيه القانون، لا تتحمل شركة Senti Bio أي التزام بتحديث أي بيانات تطلعية علنًا، سواء كان ذلك نتيجة لمعلومات جديدة أو أحداث مستقبلية أو غير ذلك.
توافر معلومات أخرى حول شركة سينتي للعلوم الحيوية القابضة.
للمزيد من المعلومات، يُرجى زيارة موقع Senti Bio الإلكتروني www.sentibio.com أو متابعة Senti Bio على منصة X (@SentiBio) ولينكدإن (Senti Biosciences). يُرجى من المستثمرين وغيرهم ملاحظة أننا نتواصل معهم ومع الجمهور عبر موقعنا الإلكتروني ( www.sentibio.com )، بما في ذلك، على سبيل المثال لا الحصر، إفصاحات الشركة، وعروض المستثمرين، والأسئلة الشائعة، والتقارير المقدمة إلى هيئة الأوراق المالية والبورصات الأمريكية، والبيانات الصحفية، ونصوص المكالمات الجماعية العامة، ونصوص البث المباشر، بالإضافة إلى منصات X ولينكدإن . قد تُعتبر المعلومات التي ننشرها على موقعنا الإلكتروني أو على منصات X أو لينكدإن معلومات جوهرية. لذا، نشجع المستثمرين ووسائل الإعلام والمهتمين على مراجعة المعلومات التي ننشرها بانتظام. لا تُعتبر محتويات موقعنا الإلكتروني أو حساباتنا على وسائل التواصل الاجتماعي مُدرجة بالإحالة في أي ملف بموجب قانون الأوراق المالية لعام 1933، بصيغته المعدلة.
للتواصل مع المستثمرين:
فريق JTC، ذ.م.م.
جينين توماس
(908) 824-0775
SNTI@jtcir.com
تتوفر صورة مرفقة بهذا الإعلان على الرابط التالي: https://www.globenewswire.com/NewsRoom/AttachmentNg/aae7bc52-613b-4390-92fc-de95dd361d1f

